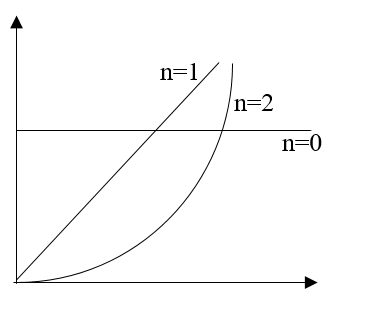
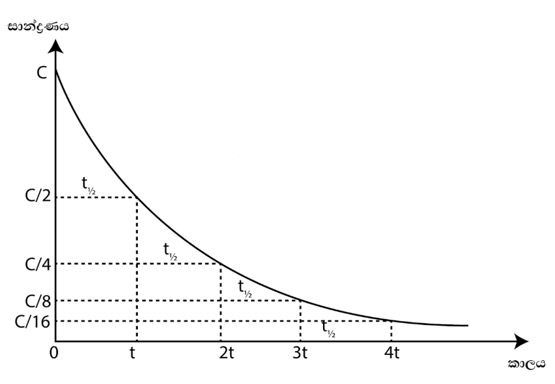
- තෝරාගත් ප්රතික්රීයක සාන්ද්රණය එහි ආරම්භක සාන්ද්රණයෙන් හරි අඩක් බවට පත් වීමට ගතවන කාලය කිසියම් ප්රතික්රියාවක අර්ධ ජීව කාලය \left(\mathrm t\;_½\right) වේ.
- ප්රතික්රියාවක දළ ශීඝ්රතාව විස්තර කිරීමට අර්ධ ජීව කාල සංකල්පය ප්රයෝජනවත්ය.
මූලික පියවර ප්රතික්රියාවක (පළමු පෙළ ප්රතික්රියාවක) අර්ධ ජීව කාලය
- පළමු පෙළ ප්රතික්රියාවක අර්ධ ජීව කාලය,
\boxed{\mathrm t\;_½=\;\frac{0.693}{\mathrm k}}
මගින් දෙනු ලැබේ.
මෙහි k යනු වේග නියතයයි.
දෙන ලද උෂ්ණත්වයකදී දෙන ලද ප්රතික්රියාවක් සදහා k නියතයක් බැවින් ද, ප්රකාශනයට කිසිදු සාන්ද්රණ පදයක් ඇතුළත් නොවන බැවින් ද, පළමු පෙළ ප්රතික්රියාවක අර්ධ ජීව කාලය ප්රතික්රියකයේ ආරම්භක සාන්ද්රණයෙන් ස්වායක්ත වූ නියතයකි.
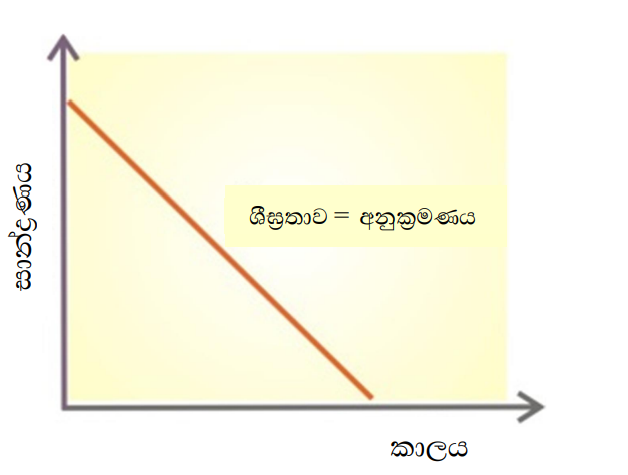
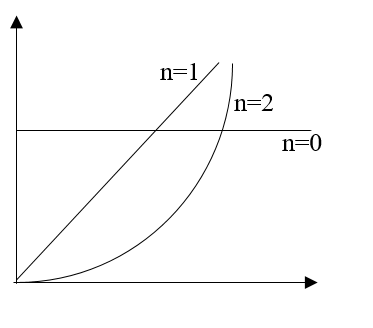
- පළමු පෙළ ප්රතික්රියාවක් සදහා R = k[A] බැවින් සාන්ද්රණය එදිරියේ R ප්රස්තාර ගත කල විට මූලය හරහා යන සරල රේඛාවක් ලැබේ.

පළමු පෙළ ප්රතික්රියාවක කාලයට එරෙහිව ශීඝ්රතාවයේ ප්රස්තාරය.
ශුන්ය පෙළ ප්රතික්රියාවක අර්ධ ජීව කාලය
{\mathrm t}_\frac12\;=\;\frac{\left[{\mathrm A}_\circ\right]}{2\mathrm k}
මගින් දෙනු ලැබේ.
[A]0 – Aහි ආරම්භක සාන්ද්රණය
k – වේග නියතය
ඉහත ප්රකාශනයට අනුව ශුන්ය පෙළ ප්රතික්රියාවක අර්ධ ජීව කාලය ආරම්භක සාන්ද්රණය මත රදා පවතී.ආරම්භක සාන්ද්රණය අඩු වන විට අර්ධ ජීව කාලය අඩු වේ.
- ශුන්ය පෙළ ප්රතික්රියාවක ශීඝ්රතාවය ප්රතික්රියකයේ සාන්ද්රණයන්ගෙන් ස්වායක්ත වේ.
R = k[A]0
R = k
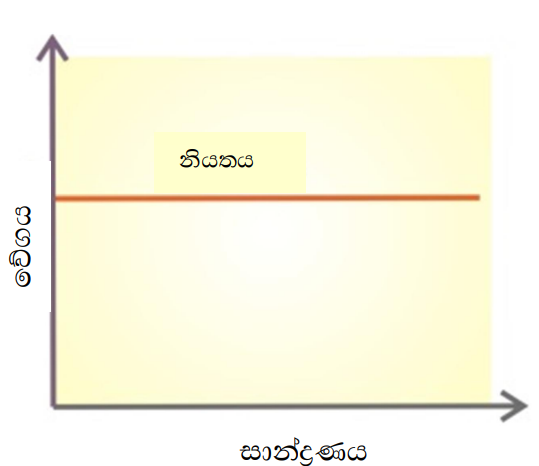
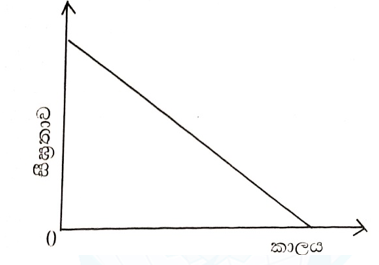
- එම නිසා ප්රතික්රියාව ප්රතික්රියා කාල සීමාව තුළදී එකම ශීඝ්රතාවයකින් සිදු වේ. ඒ අනුව ප්රතික්රීයක වැය වන ශීඝ්රතාව නියත වන අතර ප්රතික්රියකයේ සාන්ද්රණය නියත ශීඝ්රතාවයකින් අඩු වේ.
දෙවන පෙළ ප්රතික්රියාවක අර්ධ ජීව කාලය
- දෙවන පෙළ ප්රතික්රියාවකදී ප්රතික්රියාවේ අර්ධ ජීව කාලය ආරම්භක සාන්ද්රණය මත රදා පවතී.ආරම්භක සාන්ද්රණය අඩු වන විට අර්ධ ජීව කාලය වැඩි වේ.
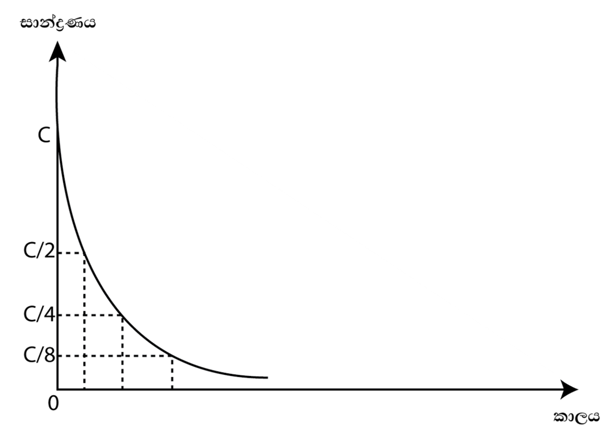
- දෙවන පෙළ ප්රතික්රියාවක් සදහා R = k [A]2 වන හෙයින් ප්රතික්රියකයේ සාන්ද්රණය එදිරියේ R ප්රස්තාරගත කළ විට ලැබෙන්නේ පරාවලයකින් කොටසකි.

පරීක්ෂණ
Na2SO3 හා HCl අතර සිදුවන ප්රතික්රියාවේ පෙළ එක් එක් ප්රතික්රීයක සංඝටක වල සාන්ද්රණයන්ට අදාලව සෙවීම.
{\mathrm{Na}}_2{\mathrm S}_2{{\mathrm O}_3}_{(\mathrm{aq})}\;+\;2{\mathrm{HCl}}_{(\mathrm{aq})}\;\rightarrow\;{\mathrm S}_{(\mathrm s)}\;+\;{\mathrm{NaCl}}_{(\mathrm{aq})}\;+\;{\mathrm{SO}}_{2(\mathrm g)}\;+\;{\mathrm H}_2{\mathrm O}_{(\mathrm{aq})}
- මෙම ප්රතික්රියාවෙන් ළා කහ පැහැති S (සල්ෆර්) අවලම්භනය සෑදේ.
- මෙහිදී නියත S (සල්ෆර්) ප්රමාණයක් ලැබීමට ගතවන කාලය සීඝ්රතාවය ලෙස භාවිතා කෙරේ.
අවශ්ය ද්රව්ය :- බීකරයක් , කළු පැහැති කතිර සළකුණක් (X) යෙදූ සුදු පැහැති කඩදාසියක්,
විරාම ඝටිකාවක් , 3.0 mol dm-3 HCl අම්ල ද්රාවණයක්,
40 g dm-3 (0.15 mol dm-3) Na2S2O3 ද්රාවණයක්.
ක්රියා පිළිවෙල:-
-
-
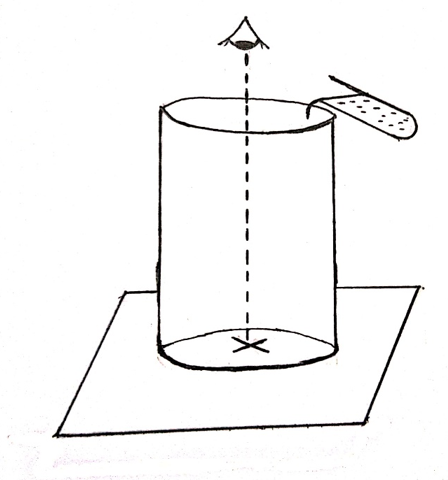
- කළු කතිරය (X) යෙදූ සුදු කඩදාසිය මත බීකරය තබන්න. පහත වගු වල දක්වා ඇති ප්රතික්රියක පරිමා බීකරයට දමන්න.
- ප්රතික්රියක මිශ්ර කරන මොහොතේම විරාම ඝටිකාව ක්රියාත්මක කල යුතු ය.
- කළු කතිරය වැසීමට ගතවන කාලය මැන ගන්න.
-
Na2S2O3 වලට අදාලව පෙළ සෙවීමට HCl සාන්ද්රණය නියතව තබා පරීක්ෂණය සිදු කිරීම.
| පරීක්ෂණ අංකය | 0.15 mol dm-3 Na2S2O3 පරිමාව / cm3 | 3 mol dm-3 HCl පරිමාව / cm3 | ආස්රැත ජලය පරිමාව | කතිර ලකුණ වැසීමට ගතවන කාලය | සීඝ්රතාවය |
| 1 | 25.0 | 5.0 | 0.0 | ||
| 2 | 20.0 | 5.0 | 5.0 | ||
| 3 | 15.0 | 5.0 | 10.0 | ||
| 4 | 10.0 | 5.0 | 15.0 | ||
| 5 | 05.0 | 5.0 | 20.0 |
HCl වලට අදාලව පෙළ සෙවීමට Na2S2O3 සාන්ද්රණය නියතව තබා පරීක්ෂණය සිදු කිරීම.
| පරීක්ෂණ අංකය | 0.15 mol dm-3 Na2S2O3 පරිමාව / cm3 | 3 mol dm-3 HCl පරිමාව / cm3 | ආස්රැත ජලය පරිමාව | කතිර ලකුණ වැසීමට ගතවන කාලය | සීඝ්රතාවය |
| 1 | 25.0 | 5.0 | 0.0 | ||
| 2 | 25.0 | 4.0 | 1.0 | ||
| 3 | 25.0 | 3.0 | 2.0 | ||
| 4 | 25.0 | 2.0 | 3.0 | ||
| 5 | 25.0 | 1.0 | 4.0 |
HCl වලට අදාලව පෙළ සෙවීමට
- පෙළ ක්රම දෙකකට සෙවිය හැක
I ක්රමය
ශ\mathrm{ීග්}\mathrm{රතාවය}\;=\;\frac{\mathrm{නියත}\;\mathrm s\;\mathrm{ප්}\mathrm{රමාණය}}{\;\mathrm{කාලය}}
\mathrm R\;\;\mathrm\alpha\;\;\frac1{\mathrm t}----(1)\;
සීඝ්රතා නියමයෙන්,
\mathrm R\;\;\mathrm\alpha\;\;\lbrack{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_3\rbrack^{\mathrm n}\;\;
මෙහි n යනු මෙම ප්රතික්රියාවේ Na2S2O3 වලට සාපේක්ෂ පෙළයි.
මුළු පරිමාව නියත නිසා,
සෝඩියම් තයෝසල්ෆේට් සාන්ද්රණය තියන තයෝසල්ෆේට් මවුල ගානට සමානුපාතිකයි. අපි මුළු පරිමාව නියත කරන නිසා අපි ද්රාවණයට දාන තයෝසල්ෆේට් පරිමාවට තියෙන තයෝසල්ෆේට් මවුල ගණන සමාන වෙනවා. මොකද අපි පිටින් දාන තයෝසල්ෆේට් ද්රාවනයේ සාන්ද්රණය නියත නිසා පිටින් දාන තයෝසල්ෆේට් මවුල ගාන ඒ දාන පරිමාවට සමානුපාතික වෙනවා.
\begin{array}{l}\mathrm C\;=\;\frac{\mathrm n}{\mathrm V}\\\mathrm n\;=\;\mathrm{CV}\\\mathrm C\;\mathrm{නියත}\;\mathrm{නිසා}\;,\;\\\mathrm n\;\;\mathrm\alpha\;\;\mathrm V\end{array}
\lbrack{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}\rbrack\;\;\mathrm\alpha\;\;\mathrm V\;_{{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\;
මෙහි \mathrm V\;_{{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\; යනු අදාල පරීක්ෂණය සදහා යොදා ගන්නා Na2S2O3 පරිමාවයි.
ඒ අනුව,
\mathrm R\;\mathrm\alpha\;\left(\;{\mathrm V}_{\;{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\right)^{\mathrm n}-----(2)
1න් හා 2න්,
\begin{array}{l}\left({\mathrm V}_{{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\right)^{\mathrm n}\;\;\;\mathrm\alpha\;\frac1{\mathrm t}\\\left({\mathrm V}_{{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\right)^{\mathrm n\;\;\;\;\;}=\;\frac{\mathrm k}{\mathrm t}\\\left({\mathrm V}_{{\mathrm{Na}}_2{\mathrm S}_2{\mathrm O}_{3(\mathrm{aq})}}\right)^{\mathrm n}\;\mathrm t\;=\;\mathrm k\end{array}
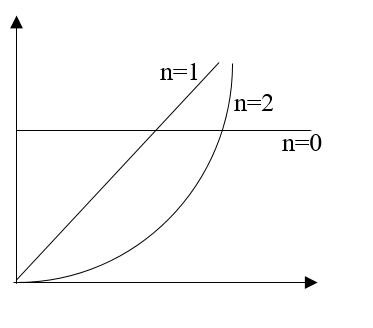
n = 0 විට t =k
n = 1 විට Vt = k
n = 2 විට V2t = k
මඟින් පෙළ සෙවිය හැක.
II ක්රමය
එක් එක් ප්රතික්රියක සංඝටක වල සාන්ද්රණය ගනණය කරන්න. සෑම පරීක්ෂණයකටම අදාලව සීඝ්රතාවය ගනණය කරන්න . ඉන් පසු Na2S2O3 සාන්ද්රණය හා ශිග්රතාවේ ප්රස්තාරය අඳින්න.
පරීක්ෂණය සාර්ථක වීමට ගත හැකි ක්රියා මාර්ග
- සෑම පරීක්ෂණයක්ම එක් පුද්ගලයෙකු විසින් සිදු කිරීම.
- සෑම පරීක්ෂණයකටම එකම පරීක්ෂණ කට්ටලය යොදා ගැනීම.
- සෑම විටක ම කතිර සලකුණ බීකරයේ මධ්ය ප්රදේශයට වන්නට තැබීම.
- සෑම විටකම ඇස එකම දිශානතියක් ඔස්සේම යොමු කිරීම.
- අවට පරිසරයේ උශ්ණත්වය නියතව තබා ගැනීම.
- සාන්ද්රණය ඉහළ ප්රතික්රියක භාවිතා කිරීම.
Fe2+ හා I– අයන අතර ප්රතික්රියාවේ පෙළ එක් එක් ප්රතික්රීයක සංඝටක වල සාන්ද්රණයන්ට අදාලව සෙවීම.
2{\mathrm{Fe}^{3+}}_{(\mathrm{aq})}\;+\;2{\mathrm I^-}_{(\mathrm{aq})\;}\rightarrow\;2{\mathrm{Fe}^{2+}}_{(\mathrm{aq})\;}+\;{\mathrm I}_{2(\mathrm{aq})}
- සෑදෙන I2 පිෂ්ඨක දර්ශක හමුවේ නිල් පැහැයට හැරේ.
- පිෂ්ඨ ද්රාවනය නිල් පැහැ වීමට තිබිය යුතු අවම I2 සාන්ද්රණය 1×10-3 moldm-3 වන අතර එය ඉතා සුලු ප්රමාණයක් බැවින් ප්රතික්රියක මිශ්ර කළ විගසම මෙම I2 සාන්ද්රණය සෑදේ.
- එම නිසා ගතවන කාලය මැනීමට අසීරු වන බැවින් කාලය මැනීමට හැකිවන පරිදි ප්රතික්රියාව සිදු කිරීමට I2 සමඟ ශීඝ්රයෙන් ප්රතික්රියා කර I– සාදන Na2SO4 නියත ප්රමාණයක් යොදාගත හැක.
2{\mathrm S}_2{{\mathrm O}_3^{2-}}_{(\mathrm{aq})}\;+\;{\mathrm I}_{2(\mathrm{aq})}\;\rightarrow\;{\mathrm S}_4{{\mathrm O}_6^{-2}}_{(\mathrm{aq})}\;+\;2{\mathrm I^-}_{(\mathrm{aq})}
- Na2S2O3අවසන් වූ මොහොතේම ද්රාවනය නිල් පැහැ වේ.
- සෑදෙන I2 ප්රමාණය යොදාගත් Na2S2O3 මඟින් නිර්ණය කරගත හැක.
- අවශ්ය ද්රව්ය :-
-
- බීකර , මිනුම්සරා , විරාමඝටිකාව
- ආම්ලික 0.1 moldm-3 හා 1 moldm-3 Fe2(SO3)3 ද්රාවණයක්
- 0.2 moldm-3 හා 3 moldm-3 KI ද්රාවණයක්
- 0.006 moldm-3 Na2S2O3 ද්රාවණයක්
-
ක්රියා පිලිවෙළ :-
ප්රතික්රීයක පහත පරිදි වෙන වෙනම බීකර දෙකකට දමා ගන්න.ඒවා මිශ්ර කරන මොහොතේම කාලය මැනීම ආරම්භ කරන්න.
බීකරය 1 – Fe2+(aq) ද්රාවණය + තනුක H2SO4
බීකරය 2 – I–(aq) + S2O3 2-(aq) + පිෂ්ටය +ආස්රැත ජලය
Fe3+(aq)ට සාපේක්ෂව පෙළ සෙවීමට
පහත වගුවේ පරිදි ප්රතික්රීයක පරිමා එකතුකර නිල් පැහැ වීමට ගතවන කාලය මැන ගන්න.
| පරීක්ෂණ අංකය | ආස්රැත ජලය / cm3 | 0.1moldm-3 ආම්ලික Fe3+(aq) ද්රාවණය / cm3 | 3 moldm-3 KI ද්රාවණය / cm3 | 0.006 moldm-3 S2O32-aqද්රාවණයක් + පිෂ්ඨය /cm3 | ද්රාවණය නිල් පැහැ වීමට ගතවන කාලය |
| 1 | 0.0 | 25.0 | 10.0 | 15.0 | |
| 2 | 5.0 | 20.0 | 10.0 | 15.0 | |
| 3 | 10.0 | 15.0 | 10.0 | 15.0 | |
| 4 | 15.0 | 10.0 | 10.0 | 15.0 | |
| 5 | 20.0 | 5.0 | 10.0 | 15.0 |
-
I–(aq) ට සාපේක්ෂව පෙළ සෙවීමට
| පරීක්ෂණ අංකය | ආස්රැත ජලය / cm3 | 0.1moldm-3 ආම්ලික Fe3+(aq) ද්රාවණය / cm3 | 3 moldm-3 KI ද්රාවණය / cm3 | 0.006 moldm-3 S2O32-aqද්රාවණයක් + පිෂ්ඨය /cm3 | ද්රාවණය නිල් පැහැ වීමට ගතවන කාලය |
| 1 | 0.0 | 25.0 | 10.0 | 15.0 | |
| 2 | 2.0 | 25.0 | 8.0 | 15.0 | |
| 3 | 4.0 | 25.0 | 6.0 | 15.0 | |
| 4 | 6.0 | 25.0 | 4.0 | 15.0 | |
| 5 | 8.0 | 25.0 | 2.0 | 15.0 |
ගනණය කිරීම්
- පෙළ ක්රම දෙකකට සෙවිය හැක
I ක්රමය
\text{සීග්රතාවය}\;=\;\frac{\text{නියත නිල් පැහැය}\;\;}{\text{කාලය}}
\mathrm R\;\mathrm\alpha\;\frac1{\mathrm t}-----(1)
සීග්රතා නියමයෙන්,
\mathrm R\;\mathrm\alpha\;\lbrack{\mathrm{Fe}^{3+}}_{(\mathrm{aq})}\rbrack^{\mathrm n}
මෙහි n යනු මෙම ප්රතික්රියාවේ Fe3+ වලට සාපේක්ෂ පෙළයි.
මුළු පරිමාව නියත නිසා,
\lbrack{\mathrm{Fe}^{3+}}_{(\mathrm{aq})}\rbrack\;\;\mathrm\alpha\;\;\mathrm V\;_{\mathrm{Fe}^{{}_{3+}}\;_{(\mathrm{aq})}}
ඒ අනුව,
\mathrm R\;\;\mathrm\alpha\;\left(\;{\mathrm V}_{\mathrm{Fe}^{3+}\;_{(\mathrm{aq})\;}}\right)^{\mathrm n}\;\;\;\;\;\;\;\;------(2)
1න් හා 2න්,
\begin{array}{l}\left({\mathrm V}_{{\mathrm{Fe}^{+3}}_{(\mathrm{aq})}}\right)^{\mathrm n}\;\;\mathrm\alpha\;\;\frac1{\mathrm t}\\\left({\mathrm V}_{{\mathrm{Fe}^{+3}}_{(\mathrm{aq})}}\right)^{\mathrm n}\;\;=\;\;\frac{\mathrm k}{\mathrm t}\\\left({\mathrm V}_{{\mathrm{Fe}^{+3}}_{(\mathrm{aq})}}\right)^{\mathrm n}\;\mathrm t\;\;=\;\mathrm k\\\end{array}
n = 0 විට t =k
n = 1 විට Vt = k
n = 2 විට V2t = k
මඟින් පෙළ සෙවිය හැක.
II ක්රමය
එක් එක් ප්රතික්රියක සංඝටක වල සාන්ද්රණය ගනණය කරන්න. ඉන්පසු ඒ ඒ අවස්තාවේ ශීග්රතාවය (1/t) ගනණය කරන්න. ශීග්රතාවය හා සාන්ද්රණය අතර ප්රස්ථාරය ඇඳීමෙන් පෙළ සෙවිය හැක.
මැග්නීසියම් (Mg) හා සල්ෆියුරික්(H2SO4) අතර සිදුවන ප්රතික්රියාවේ H+ සාන්ද්රණයන්ට සාපේක්ෂව පෙළ සෙවීම .
- සල්ෆියුරික් සාන්ද්රණයන් වෙනස් කරමින් නියත H2 පපරිමාවක් ලැබීමට ගත වන කාලය මැනීම මගින් Hට සාපේක්ෂකව පෙළ සෙවිය හැක.
- අවශ්ය ද්රව්ය :-
-
- කැකෑරුම් නලය
- කැකෑරුම් නලයට සවි කල හැකි සිදුරක් සහිත රබර් ඇබය.
- සිදුරට සරිලන දිගැති වීදුරු බටය
- විරාම ඝටිකාව
- රබර් වළලු
- බීකරය
- 1.0moldm-3 HCl අම්ල ද්රාවණය
- 3cm දිග පිරිසිදු කරන ලද Mg පටිය
-
- ක්රියාපිළිවල
-
- කැකෑරුම් නලයට ජලය 10cm3 ක් දමා ද්රාවණය මට්ටම රබර් වළලු මගින් ක්රමාංකනය කරනු ලැබේ.
- ජලය ඉවත් කර නලයට අවශ්ය HCl පරිමාව දමා සම්පූර්ණයෙන් ජලය පුරවනු ලැබේ.
-
-
-
- පිරිසිදු කරන ලද Mg පටිය සහිත ඇබය පහත ආකරයට සවි කර Mg පටිය ඇතුල් වන පරිදි මූඩිය වසා යටිකුරු කරමින් විරාම ඝටිකාව ක්රියා කරවීම එකවර සිදු කරනු ලැබේ.
-
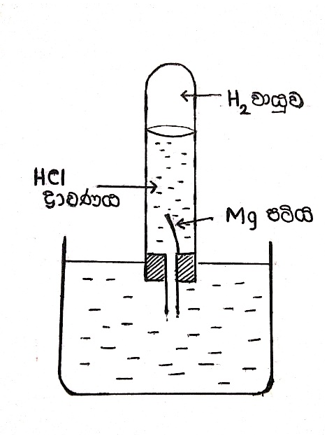
- පහත දැක්වෙන ආකාරයට අම්ල පරිමා භාවිතා කරමින් නියත හයිඩ්රජන් පරිමාවක් ලැබීමට ගතවන කාලය මැන ගනු ලැබේ.
| පරීක්ෂණ අංකය | 1mol dm-3 HCl පරිමාව / cm3 | නියත H2 පරිමාවක් ලැබීමට ගතවන කාලය |
| 1 | 40.00 | |
| 2 | 35.00 | |
| 3 | 30.00 | |
| 4 | 25.00 | |
| 5 | 20.00 |
- සීග්රතාවය හා [H+] අතර ප්රස්තාරය ඇදීමෙන් පෙළ සෙවිය හැක.