හැඳින්වීම
පරමාණුක වාදය ස්ථාපිත වීමටත් ප්රථම මූලද්රව්ය හා සංයෝග අතර වෙනස්කම් සැකයෙන් තොරව සනාථ විය. රසායනික සංයෝග සෑදෙන්නේ මූලද්රව්ය දෙකක් හෝ කීපයක් රසායනිකව සංයෝජනය වීමෙනි. මෙම සංයෝග සෑදීමේදි ඒවායේ බන්ධන ස්වභාවය පිළිබඳ ප්රශ්න ගණනාවක් ඉස්මතු විය.
- සංයෝග වල පරමාණු බන්ධනය වී ඇත්තේ කෙසේද?
- සංයෝග වල පරමාණු අතර හා ඒවා අතර ඇති ආකර්ෂණ බල මොනවාද?
- ජලයෙහි H2O සූත්රය OH මිස නොවන්නේ මන්ද? සෝඩියම් ක්ලෝරයිඩ් වල සුත්රය NaCl මිස NaCl2 නොවන්නේ ඇයි?
- සෝඩියම් ක්ලෝරයිඩ් ජලයේ දියවන අතර ද්රාවණය විද්යුතය සන්නායනය කරයි. එහෙත් කාබන් ටෙට්රාක්ලෝරයිඩ් ජලය හා අමිශ්ර වන අතර විද්යුතය සන්නයනය නොකරයි.
මේවාට පිලිතුර මෙවැනි සංයෝගවල රසායනික බන්ධන ස්වභාවය මත රදාපවතින බවයි.
සමහර මූලද්රව්යවල පරමාණු ඉලෙක්ට්රෝන ඉවත් කර උච්ච වායු වින්යාසය ලබා ගන්නා අතර සමහර මූලද්රව්යවල පරමාණු ඉලෙක්ට්රෝන ලබාගෙන උච්ච වායු වින්යාසය ලබාගනි. මෙලෙස ඉලෙක්ට්රෝන ප්රතිසංවිධානය වීම හේතුවෙන් පරමාණු අතර ඇතිවන ආකර්ෂණ බල රසායනික බන්ධන ලෙස හැඳින්වේ.
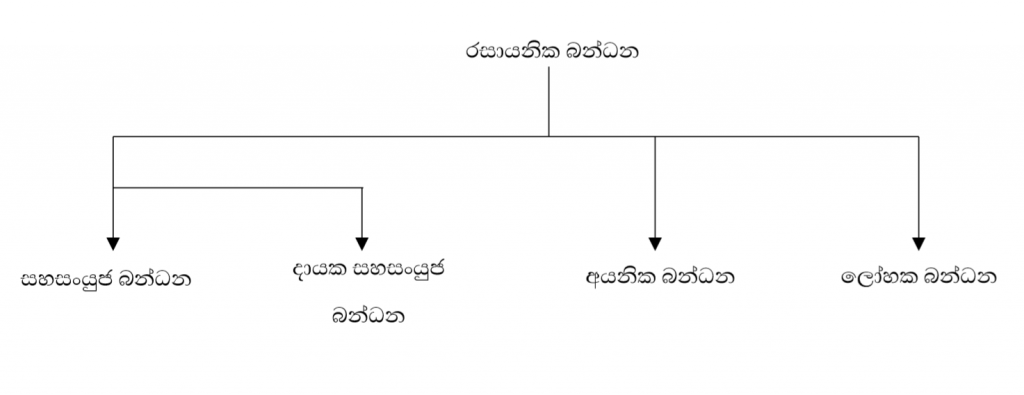
ඉදිරියේදී ප්රශ්න ඇතුලත් වන්නේ මෙතනටයි.



