ඇල්කිල් හේලයිඩ නිපදවීම
- ඇල්කීනයක් හෝ ඇල්කයිනයක් හැලජන දියර සමඟ ප්රතික්රියාවේදී එම ඇල්කීනයේ හෝ ඇල්කයිනයේ පවතින π බන්ධනය බිඳ වැටී හැලජන පරමාණු ආකලනය වීම සිදුවේ.
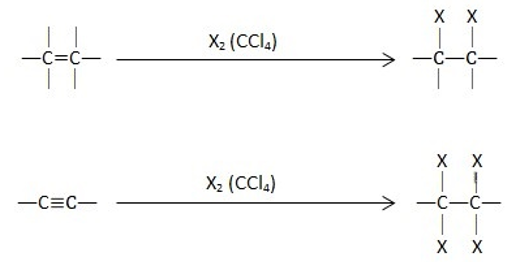
- ඇල්කීනයක් හෝ ඇල්කයිනයක් හයිඩ්රජන් හේලයිඩ සමඟ ප්රතික්රියාවේ දී ඒවායේ π බන්ධන බිඳ වැටී HX අණුව ආකලන වීමෙන් ඇල්කිල්හේලයිඩ ලබාගත හැක. මෙහිදී HX අණුව ආකලනය වන ස්වරූපය ප්රතික්රියා මාධ්යය මත තීරණය වේ.
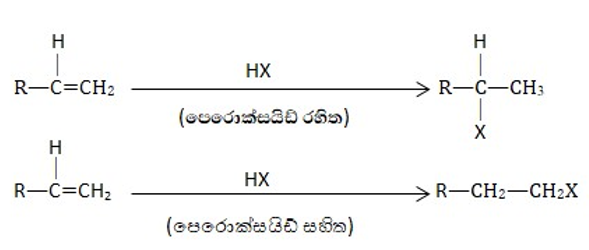
- පෙරොක්සයිඩ හමුවේ HBr හි පමණක් දිශාව වෙනස් වේ.HCl, HI ආකලනය වීමේ දී දිශාව වෙනස් නොවේ.
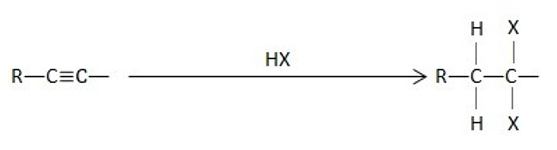
- විසරිත හිරු එළිය ඇති පරිසරයකදී ඇල්කේන හා නිදහස් හැලජන ප්රතික්රියා කරවීමෙන් හයිඩ්රජන් පරමාණු වෙනුවට හැලජන පරමාණු සම්බන්ධ වේ.
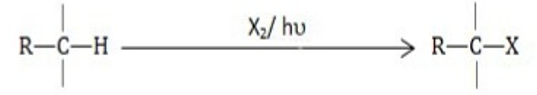
- මෙහෙදී දාම ප්රතික්රියාවක් සිදුවෙමින් ඵල මිශ්රණයක් ලබා දෙයි.එහි ප්රාථමික,ද්විතියික හා තෘතීක ඵල සියල්ල අඩංගු වේ.
- නිර්ජලීය තත්ත්ව යටතේ Fe, FeCl3, FeBr3, AlCl3, AlBr3 වැනි ලුවිස් අම්ල හමුවේදී බෙන්සීන් Cl2, Br2 සමග ප්රතික්රියා කරන විට බෙන්සීන් වලට හැලජන පරමාණුවක් ආදේශ වේ.
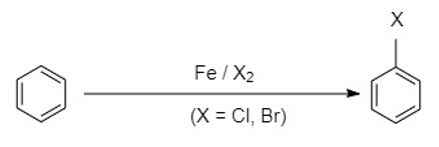
- ප්රාථමික, ද්විතීයික, තෘතීයික මධ්යසාර හා බෙන්සිල් මධ්යසාර පොස්පරස් හේලයිඩ සමග රත් කලවිට OH ඉවත් වී හැලජනය ආදේශ වේ.

ඇල්කොහොලයක්, PX3 ස්වරූපයේ සංයෝගයක් සමඟ ප්රතික්රියා කර වූ විට අතුරුඵල වශයෙන් H3PO3 ද PX5 ස්වරූපයේ සංයෝගයක් සමඟ ප්රතික්රියා කර වූ විට අතුරුඵල වශයෙන් POX3 හා HX ද ලැබේ.
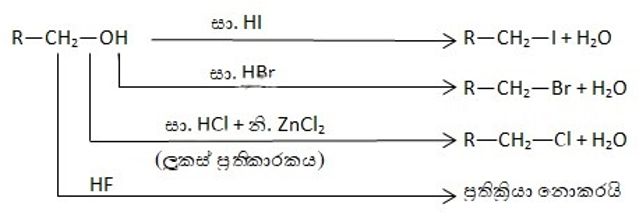
- ප්රාථමික, ද්විතීයික, තෘතීයික මධ්යසාර හා බෙන්සිල් මධ්යසාර HI, HBr සමග රත් කලවිට OH ඉවත් වී හැලජනය ආදේශ වේ. එහෙත් සාන්ද්ර HCl සමග මේ ආකාරයට ප්රතික්රියා නොකරයි. ඒ සඳහා නිර්ජලීය ZnCl2 උත්ප්රේරකයක් ලෙස යෙදිය යුතුය. HF සමග ප්රතික්රියාවක් සිදු නොවේ.
- ඇල්කොහොලයක් හා SOCl2 අතර ප්රතික්රියාවේ දී එම ඇල්කොහොලයේ ඇති OH කාණ්ඩය Cl පරමාණුවක් මගින් ආදේශ වීම දක්නට ලැබේ.

මෙහිදී අතුරුඵල ලෙස SO2 හා HCl සෑදෙනු ඇත.
**නව විෂය නිර්දේශය යටතේ මෙම කොටස අදාල නොවේ.
ඇල්කිල් හේලයිඩ වල භෞතික ගුණ
- එකම කාබන් සංඛ්යාවක් ඇති ඇල්කිල් ක්ලෝරයිඩයේ සිට ඇල්කිල් අයඩයිඩය කරා යාමේදී C-X ධ්රැවීයතාවය අඩුවී ද්විධ්රැව – ද්විධ්රැව ආකර්ෂණ බලයේ ප්රබලතාවය අඩුවේ. මේ නිසා ද්රවාංක තාපාංක අඩු විය යුතු නමුත් Cl– සිට I– කරා යාමේදී සාපේක්ෂ අණුක ස්කන්ධය හා ක්ෂේත්රඵලය වැඩිවීමට අනුරූපව ද්රවාංක තාපාංක වැඩිවේ.
- එකම කාබන් සංඛ්යාවක් ඇති හයිඩ්රොකාබනයට වඩා ඇල්කිල් ක්ලෝරයිඩය හා ඇල්කිල් ෆ්ලුවෝරයිඩය වල ධ්රැවීයතාවය වැඩිවී ද්විධ්රැව- ද්විධ්රැව ආකර්ෂණ බලයේ ප්රබලතාවය වැඩිවේ. එම නිසා ද්රවාංක තාපාංක වැඩිවේ.
එහෙත් R-Br හා R-I වල C-X ධ්රැවීයතාවය හයිඩ්රොකාබනයට වඩා අඩුය. නමුත් හයිඩ්රොකාබනයට සාපේක්ෂව R-Br හා R-I වල සාපේක්ෂ අණුක ස්කන්ධය හා ක්ෂේත්රඵලය වැඩි නිසා ද්රවාංක තාපාංක වැඩිවේ.
- ඇල්කිල් හේලයිඩ වල C-X බන්ධනය ධ්රැවීය වුවද එම ධ්රැවීයතාවය ජලය සමඟ හයිඩ්රජන් බන්ධන සෑදීමට ප්රමාණවත් නොවේ. එමනිසා ඇල්කිල් හේලයිඩ ජලයේ අද්රාව්ය වන අතර කාබනික ද්රාවකවල හොඳින් දියවේ.
ඇල්කිල් හේලයිඩ වල රසායනික ගුණ
- SN (නියුක්ලියෝෆිලික ආදේශ) ප්රතික්රියා
- ඉවත්වීමේ ප්රතික්රියා
- කාබනික ලෝහමය සංයෝග සෑදීම
SN (නියුක්ලියෝෆිලික ආදේශ) ප්රතික්රියා
- ඇල්කිල් හේලයිඩ වලට ලාක්ෂණික ප්රතික්රියා වේ.
- ඇල්කිල් හේලයිඩයේ C-X බන්ධනය ධ්රැවීය වීමට අනුව C ට ලැබෙන්නේ ∂+ ය. C වල විද්යුත් ඍණතාවය සාපේක්ෂව ඉහළ නිසා මෙහි ∂+ පවත්වාගැනීම අස්ථායි ය. මේ නිසා මෙය ඉතා පහසුවෙන්ම එකසර ඉලෙක්ට්රෝන යුග්ම සහිත අණුවක් හෝ අයනයක් (නියුක්ලියෝෆිලිකය) ආකර්ෂණය කරගනිමින් C-X බන්ධනය හැලජනය දෙසට කඩා නියුක්ලියෝෆිලිකය ආදේශ කර ගනි.
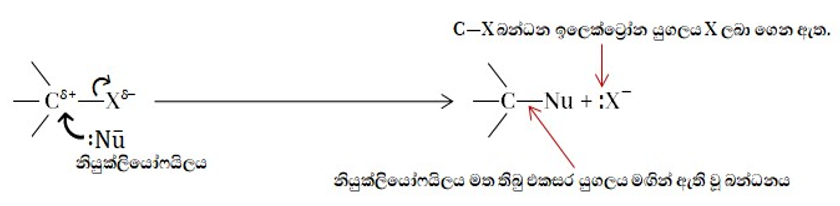
- SN ප්රතික්රියතාවයන් ප්රාථමික, ද්විතීයික, තෘතීයික ඇල්කිල්හේලයිඩ වල පහත ආකාරයට වෙනස් වේ.

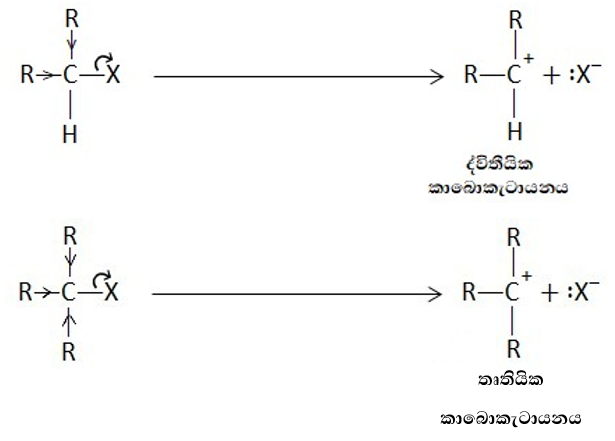
- ප්රාථමික සිට තෘතීයික කරා යාමේදී R කාණ්ඩ වලින් ඉලෙක්ට්රෝන විකර්ෂණය වැඩි වන නිසා C-X බන්ධනය හැලජනය දෙසට බිඳීම වැඩිවේ.
- මීට අමතරව C-X බන්ධනය බිඳීමෙන් සෑදෙන අතරමැදි කාබොකැටායනය ප්රාථමික සිට තෘතීයික කරා යාමේදී ස්ථායි බව වැඩිවේ.මේ අනුව,
- C-X බන්ධනය බිඳී යාමෙන් සෑදෙන තෘතීයික කාබොකැටායනයේ ඉහල ස්ථායිතාවය නිසා තෘතීයික ඇල්කිල්හේලයිඩයකදී ප්රතික්රියා යාන්ත්රණය පියවර 2 කින් සිදුවේ.
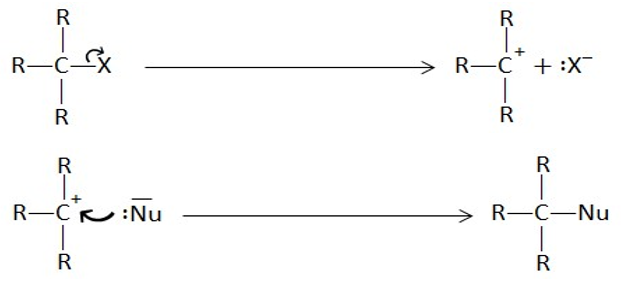
-
- C-X බන්ධනය බිඳී යාමෙන් සෑදෙන ප්රාථමික කාබොකැටායනය සාපේක්ෂව අස්ථායි නිසා ප්රාථමික ඇල්කිල්හේලයිඩයකදී ප්රතික්රියා යාන්ත්රණය තනි පියවර වේ.

- ද්විතීයික ඇල්කිල්හේලයිඩයක් විසින් සිදුකරනු ලබන SN ප්රතික්රියා යාන්ත්රණය ප්රතික්රියා තත්වය මත තීරණය වේ.
- මේ නිසා ප්රාථමික, ද්විතීයික, තෘතීයික කරා යාමේදී ඇල්කිල්හේලයිඩ වල SN ප්රතික්රියාකාරීත්වය වැඩිවේ.
- තෘතීයික ඇල්කිල්හේලයිඩ වල එම බන්ධනය බිඳීමේ පහසුතාවය නිසාම එය ස්වභාවයේ පවතින්නේ පහත ආකාරයට භාගිකව අයනීකරණය වීමෙනි.
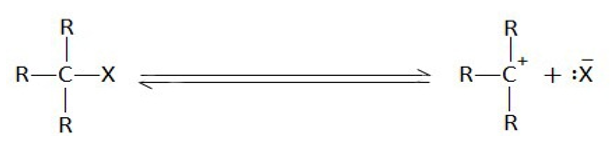
මේ හේතුව නිසාම තෘතීයික ඇල්කිල්හේලයිඩ ජලීය AgNO3 සමග අවක්ෂේප සාදයි.
ඇරිල් හේලයිඩ
ඇරිල් හේලයිඩවල හැලජනයේ ඇති එකසර ඉලෙක්ට්රෝන යුග්ම බෙන්සීන් හි π ඉලෙක්ට්රෝන වලාව සමග එක්වීමෙන් පහත සම්ප්රයුක්ත ව්යුහ හටගනී.
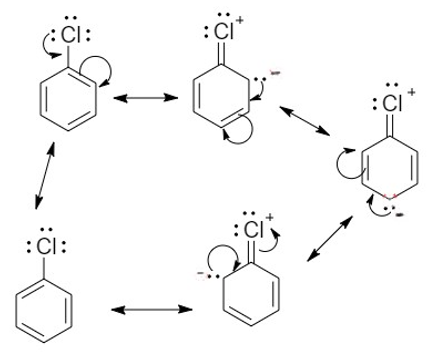
- ඇරිල් හේලයිඩවල C-X බන්ධනය ආංශික ද්විත්ව බන්ධන වල ලක්ෂණ ගනී. එබැවින් එය බිඳීම අපහසු වේ.
- මීට අමතරව ඇරිල් හේලයිඩ වල C-X බන්ධනයේ ඇති C වල මුහුම්කරණය SP2 ය. එබැවින් මෙම බන්ධනය ඇල්කිල්හේලයිඩ වලට වඩා කෙටිය.
මේ හේතු දෙකටම අනුව ඇරිල් හේලයිඩ වල C-X බිඳීම අපහසු වේ. ඒ සඳහා ඉහළ තත්ත්ව යෙදිය යුතුවේ. මේ නිසා ඇරිල් හේලයිඩ වල SN ප්රතික්රියා සාමාන්ය තත්ත්ව යටතේ දී සිදු නොවේ.
බෙන්සිල් හේලයිඩ
බෙන්සිල් හේලයිඩ වල C-X බන්ධනය බිඳීමෙන් ලැබෙන බෙන්සිල් කැටායනයට පහත ආකාරයේ සම්ප්රයුක්ත ව්යුහ පවතී.
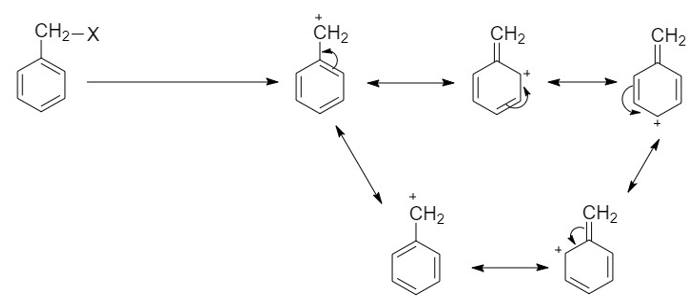
මේ නිසා බෙන්සිල් කැටායන තෘතීයික කාබොකැටායනයටත් වඩා ස්ථායී වේ. එබැවින් තෘතීයික කාබොකැටායනයකට වඩා පහසුවෙන් SN ප්රතික්රියාවකට සහභාගී වේ.
(එමෙන්ම තෘතීයික ඇල්කිල්හේලයිඩ ආකාරයටම ඊටත් වඩා පහසුවෙන් බෙන්සිල් හේලයිඩ AgNO3(aq) සමග අවක්ෂේප සාදයි.)
වයිනයිල් හේලයිඩ
වයිනයිල් හේලයිඩ වලට හැලජනයේ ඇති එකසර ඉලෙක්ට්රෝන පහත ආකාරයට C වෙතට විස්ථානගත වීමෙන් සම්ප්රයුක්ත ව්යුහ දෙකක් ඇති වේ.
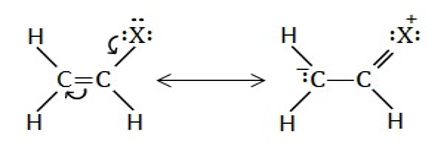
- මේ නිසා මෙහිදී ද C-X බන්ධනය ආංශික ද්විත්ව බන්ධන ලක්ෂණ ගනියි.
- එමෙන්ම මෙහිදී ද C-X බන්ධනයේ ඇති C වල මුහුම්කරණය SP2 ය. එබැවින් මෙම බන්ධනය කෙටියි.
මේ හේතු දෙකටම අනුව වයිනයිල් හේලයිඩ SN ප්රතික්රියාවන් සිදු කරන්නේ ඉහළ තත්ත්ව යටතේ දී ය.
1. ජලීය KOH (ක්ෂාර) සමග ප්රතික්රියාව
මෙහිදී හැලජනය ඉවත් වී OH– ආදේශ වීම සිදුවේ. ප්රාථමික ඇල්කිල්හේලයිඩ තනි පියවරකින් ද තෘතියික ඇල්කිල්හේලයිඩ පියවර දෙකකින් ද ප්රතික්රියාව සිදුවේ.
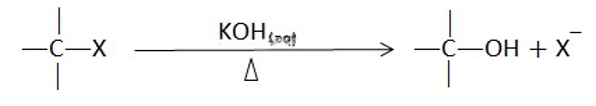
විස්තරාත්මකව දැනගැනීමට :
[youtube https://www.youtube.com/watch?v=Tk2pVG4skxs]
2. ජලීය මධ්යසාරීය KCN සමග ප්රතික්රියාව
මෙහිදී ජලීය KCN භාවිතා කලේ නම් එය විඝටනයෙන් ලැබෙන CN– අයන පහත ආකාරයට ජලවිච්ඡේදනය විය හැක.
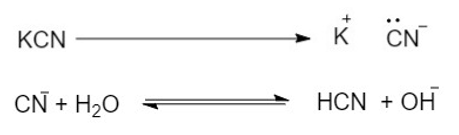
මේ අනුව මෙවැනි අවස්ථාවල CN– අමතරව OH– ද ආදේශ විය හැක. එය වළක්වාගැනීම සඳහා KCN ඉතා අවම ජල පරිමාවක දියකර වැඩිපුර මධ්යසාරය යෙදීම සිදු කරයි.
සියලු ඇල්කිල්හේලයිඩ හා බෙන්සිල් හේලයිඩ ජලීය මධ්යසාරීය KCN සමග ප්රතික්රියා කර X– ඉවත් වී CN– ආදේශ කර ගනී.
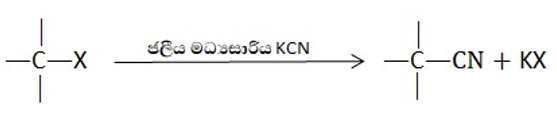
- CN– ආදේශ වීම පරිවර්තන සඳහා ඉතා වැදගත් වේ. මෙයට හේතු වන්නේ,
-
- අකාබනික ලෙස කාබන් දාමයේ දිග වැඩි කරගත හැකිය.
- CN- කාණ්ඩය පහත ආකාරයට ඉතා පහසුවෙන් වෙනත් කාණ්ඩ බවට පත් කළ හැකිය.
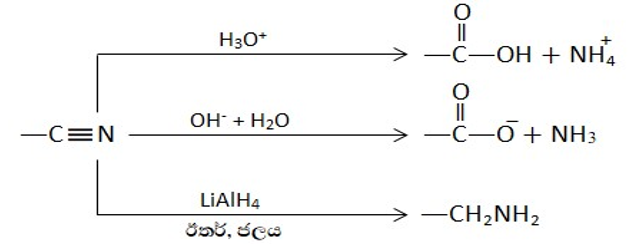
3. ඇසිටලයිඩ් ඇනායන සමග ප්රතික්රියාව
මෙම ආදේශ ප්රතික්රියාව සිදුවනුයේ කාබන් දාම දෙකක් එකට එකතුවීම සඳහාය.
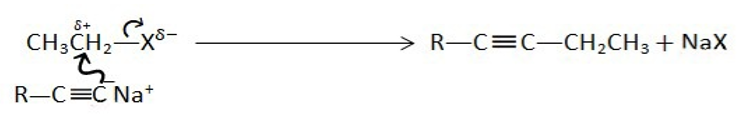
4. ඇල්කොක්සයිඩ් ඇනායන සමග ප්රතික්රියාව
සියලුම ඇල්කොහොල Na වැනි සක්රීය ලෝහයක් සමග ප්රතික්රියා කර ඇල්කොක්සයිඩ් ඇනායන සාදයි.
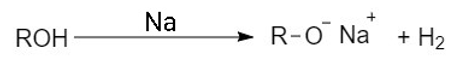
සියලුම ඇල්කිල්හේලයිඩ හා බෙන්සිල් හේලයිඩ ඇල්කොක්සයිඩ් ඇනායන සමග ප්රතික්රියා කර ඊතර සාදයි.
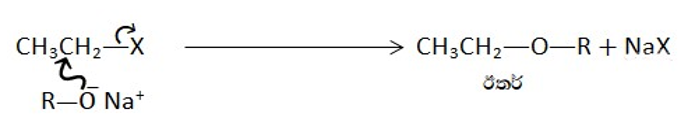
5. NH3 සමග ප්රතික්රියාව
ප්රාථමික, ද්විතීයික, තෘතීයික ඇල්කිල්හේලයිඩ හා බෙන්සිල් හේලයිඩ වැඩිපුර NH3 සමග ප්රතික්රියාවෙන් ප්රාථමික ඇමීන සාදයි.
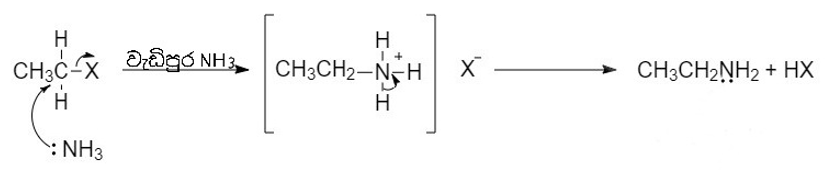
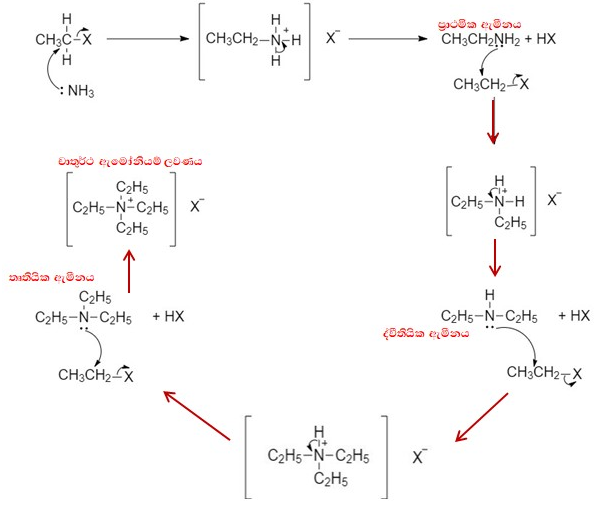
ඇල්කිල්හේලයිඩය වැඩිපුර තිබුණි නම් මෙම ප්රතික්රියාව දිගින් දිගටම සිදු වී ද්විතීයික ඇමීන, තෘතීයික ඇමීන හා චාතුර්ථ ඇමෝනියම් ලවණ දක්වා ප්රතික්රියාව සිදුවිය හැක.
b. ඉවත්වීමේ ප්රතික්රියා
ඇල්කිල්හේලයිඩවල C-X බන්ධනයේ ඉලෙක්ට්රෝන හැලජනය දෙසට ඇදී යාම නිසා එය වටා ඇති C පරමාණු වල හයිඩ්රජන් H+ ලෙස ඉවත් වීමේ නැඹුරුතාවක් පෙන්වයි.
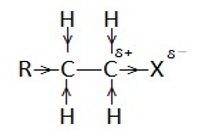
හැලජන සම්බන්ධ වී ඇති C පරමාණුවෙන් H ඉවත් වූ විට ස්ථායී සංයෝග නොසෑදේ. නමුත් ඊට යාබද C පරමාණුවෙන් H+ අයනයක් ඉවත් වූ විට ස්ථායි සංයෝග සෑදේ.
උදාහරණ : මධ්යසාරීය KOH, ඇල්කොක්සයිඩ් ඇනායන වැනි නියුක්ලියෝෆයිලයක් ඇති විටදී හැලජනය හේලයිඩයක් ලෙස ඉවත් වී ඇල්කීනයක් ප්රතිඵලය ලෙස ලැබේ.
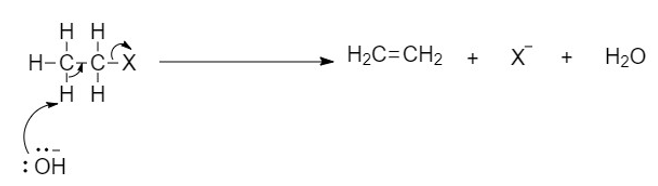
c. කාබනික ලෝහමය සංයෝග සෑදීම (ග්රීනාඩ් ප්රතිකාරකය සෑදීම)
ඇරිල්, බෙන්සිල් යනාදී සියලුම හේලයිඩ වියලි ඊතර මාධ්යයේදී Mg කුඩු සමග ප්රතික්රියා කර කාබනික ලෝහමය සංයෝග සාදයි.
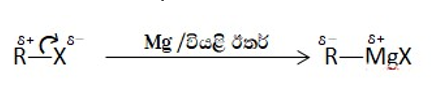
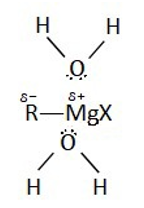
සියලුම ග්රීනාඩ් ප්රතිකාරක ජලය වැනි කුඩා H+ ප්රභවයක් සමඟ පවා ප්රතික්රියා කර හයිඩ්රොකාබන නිදහස් කරයි. මෙය වැලැක්වීම සඳහා ග්රීනාඩ් ප්රතිකාරකය ඇති මාධ්යයට හැමවිටම ජලයෙන් පවා තොර කිරීම සඳහා වියළි ඊතර මාධ්යයක් සකස් කරයි.
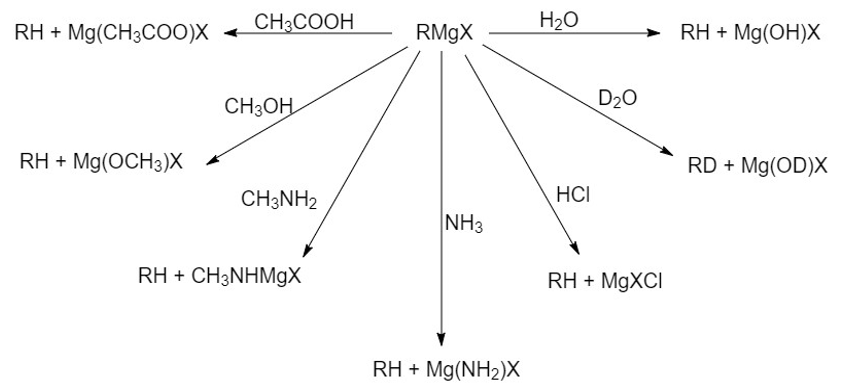
ප්රතික්රියා සම්බන්ධව තවත් විස්තර දැන ගැනීමට :

