- ජෛව රසායනික ප්රතික්රියා හා පාරිසරික ක්රියාවලි සදහා දායක වීම සහ ප්රතික්රියා සදහා ද්රාවකය ලෙස කටයුතු කිරීම ජලය සතු විශේෂ ගුණාංගයකි.
- ජල අණුවේ ජ්යාමිතික හැඩය කෝණික හැඩයක් ගනී.
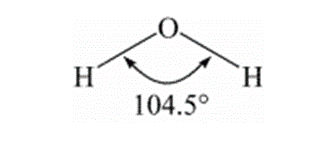
- ජල අණුව සෑදීමට හේතු වූ H හා O පරමාණුවල විද්යුත් ඍණතා වෙනස නිසා ජල අණුවේ O-H බන්ධනය ධ්රැවීය වේ.
- මෙම ධ්රැවීය O-H බන්ධන යුගලය අවකාශයේ කෝණිකව පිහිටන බැවින් ජල අණුවට සම්ප්රයුක්ත ධ්රැවීයතාවයක් ඇත.
- මෙය ඩෙමායි ඒකක 1.85(1.85D) පමණ වන නිසා ජල අණුව ප්රභල ධ්රැවීය අණුවකි.
- ඒ නිසා අණු අතර ප්රභල හයිඩ්රජන් බන්ධන හට ගැනීම නිසා ජලය කාමර උෂ්ණත්වයේදි ද්රවයකි.
- ජලයේ ප්රබල ධ්රැවීයතාවය නිසා බොහෝ සංයෝග ජලයේ ද්රාවණය වේ.
- මෙම තත්වය නිසා අහිතකර ධ්රැවීය සංයෝග ජලයේ දියවී ජලය දූෂණයට ලක්වීම පෙන්වා දිය හැකි අහිතකර ලක්ෂණයකි.
- විවිධ සංයෝග ජලයේ දියවී අදාළ කාර්ය සඳහා සුදුසු නොවීම ජලය දූෂණය නම් වෙයි.
- නිර්ධ්රැවීය සංයෝගද සුලු වශයෙන් ජලයේ දිය වන අතර මෙවැනි සමහර සංයෝග ඉතා විෂ සහිත වන අතර අංශු මාත්ර ප්රමාණවලින් ද්රාවණය වුවද අහිතකර භාවය ඉතා විශාල විය හැකිය.
- මීට අමතරව සම්පූර්ණයෙන්ම නිර්ධ්රැවීය සංයෝගයක් වන ඔක්සිජන් සුලු වශයෙන් ජලයේ දිය වෙයි.මෙය ජලජ ජෛව ක්රියාවලි සදහා අත්යවශ්ය සාධකයකි.
ජල චක්රය හා ජල දූෂණය
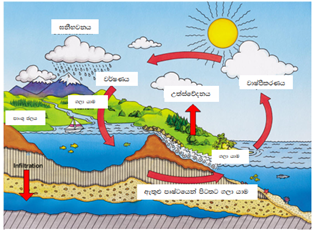
- වාෂ්පීකරණය මගින් වායුගෝලයට එක්වන ජලය ජල ගෝලයේ පිරිසිදුම ජලයයි.මෙසේ සිදුවන්නේ ජලයේ දිය වී ඇති බොහෝ ධ්රැවීය සංයෝගවල තාපාංකය ඉහළ අගයක් ගන්නා බැවින් එම සංයෝග ජලයේ වාෂ්පීකරණයත් සමඟ වායුගෝලයට ගමන් නොකරන නිසාය.
- නමුත් වායුගෝලයේ දී විවිධ රසායනික සංයෝග ජලය ද්රාවණයවේ.(H2S, NH3, NO2, SO2, H2SO4, HNO3, NH4NO3)
- වායුගෝලීය ජලය වර්ෂණය මගින් පෘථිවි පෘෂ්ඨය කරා ළඟාවේ.(වර්ෂාව, හිම, තුහින ,මීදුම, අයිස් කැට වර්ෂා ලෙස)
- එම ජලයෙන් කොටසක් පෘථිවි පෘෂ්ඨය මත ගලා යාම හේතුවෙන් තවදුරටත් දූෂණයට ලක්වෙයි.
- ඛනිජ වර්ග දිරාපත් වීමෙන් සෑදෙන ලවණ,පසේ ඇති විවිධ ලවණ, මිනිසා විසින් නිෂ්පාදනය කරන ලද රසායනික ද්රව්ය ජලයේ දිය වන බැවිනි.
- ජල චක්රයේ තවත් කොටසක් පෘථිවි අභ්යන්තරය ද පවතින අතර මෙම ජලය ද ඛණිජ සහ ලවණ දිය වීම නිසා දූෂණ තත්වයකට ලක්වෙයි.
ජල තත්ත්ව පරාමිති
- ජලයේ ධ්රැවිය හා නිර්ධ්රැවීය බොහෝ දේ ද්රාවණය වෙයි.නමුත් සමහර සංයෝග කෙතරම් ජලයේ ද්රාවණය වුවද එහි කිසිදු අහිතකර තත්ත්වයක් නැත(NaCl).නමුත් සමහර ද්රව්ය කුඩා ප්රමාණයක් දිය වුවද ඉතාම විෂ සහිතය.(උදා:- බැර ලෝහ අයන)
- එම නිසාවෙන් ජලයේ ප්රයෝජ්ය යෝග්යතාවය මැන බැලීමට ජලයෙහි ද්රාවණය වී ඇති හෝ නොවී පවතින ද්රව්ය වල උපරිම මට්ටම සහ අවම මට්ටම් පරාස තීරණය කර ඇත.
- මේවා පානීය ජලය සදහා වන රසායනික පරාමිති සහ අපජලය බැහැර කිරීම සඳහා වන පරාමිති ලෙස භාවිත කළ හැක.
|
පරාමිතිය |
ඒකකය |
උපරිම අගය හෝ පරාසය |
|
වර්ණය |
හේසල් ඒකක (Hazen Units) |
15 |
|
ආවිලතාව |
නෙෆෙලෝමෙට්ටික් අවිලතා ඒකකය ( NTU ) |
2 |
|
pH අගය |
|
6.5-8.5 |
|
රසායනික ඔක්සිජන් ඉල්ලුම |
mg L-1 |
10 |
|
පූර්ණ ද්රාවිත ඝන ද්රව්ය |
mg L-1 |
500 |
|
ජලයේ කඨිනත්වය( CaCO3ලෙස) |
mg L-1 |
250 |
|
මුළු පොස්ෆෙට්(PO42-ලෙස) |
mg L-1 |
2.0 |
|
ආසනික්(As3+ලෙස) |
mg L-1 |
0.01 |
|
කැඩ්මියම්(Cd2+ලෙස) |
mg L-1 |
0.003 |
|
ලෙඩ්(Pb2+ලෙස) |
mg L-1 |
0.01 |
|
ම’කරි( Hg+ සහ Hg2+ ලෙස) |
mg L-1 |
0.001 |
ඉදිරියේදී ප්රශ්න ඇතුලත් වන්නේ මෙතනටයි.

