ගිබ්ස් ශක්තිය (G)
- පද්ධතියක් සතු ප්රයෝජනවත් කාර්යයක් සඳහා භාවිත කළ හැකි ශක්තිය එම පද්ධතියේ ගිබ්ස් ශක්තිය ලෙස හැදින්වේ .
- SI ඒකකය = J
- භාවිතා වන ඒකකය = kJ
- ගිබ්ස් ශක්තිය විත්ති ගුණයක් වන අතර ද්රව්ය ප්රමාණයෙන් බෙදූ විට ලැබෙන මවුලික ගිබ්ස් ශක්තිය ඝටනා ගුණයක් වේ.
- SI ඒකකය = Jmol
- භාවිතා වන ඒකකය = kJmol-1
සම්මුතියක් වශයෙන් පද්ධතියක ගිබ්ස් ශක්තිය ඉදිරිපත් කෙරෙන්නේ මවුලික ගිබ්ස් ශක්තියක් වශයෙනි .
ගිබ්ස් ශක්ති විපර්යාසය (∆G)
- ප්රතික්රියාවක් සිදුවීමේදී ගිබ්ස් ශක්තියේ සිදුවන වෙනසයි .
- ගිබ්ස් ශක්තිය අවස්ථා ශ්රිතයක් වන බැවින් ඵලවල ගිබ්ස් ශක්තීන්ගේ එකතුවෙන් ප්රතික්රියකවල ගිබ්ස් ශක්තීන්ගේ එකතුව අඩු කළ විට ප්රතික්රියාවේ ගිබ්ස් ශක්ති විපර්යාසය ලැබේ .
සම්මත ගිබ්ස් ශක්තිය (Gᶿ)
- සම්මත අවස්ථාවේ පවතින පද්ධතියක් සතු ගිබ්ස් ශක්තිය යි
සම්මත ගිබ්ස් ශක්ති විපර්යාසය (∆Gᶿ)
- සම්මත අවස්ථාවේ සිදුවන ප්රතික්රියාවක ගිබ්ස් ශක්ති විපර්යාසයයි .
- ප්රතික්රියාවක ඵලවල සම්මත ගිබ්ස් ශක්තීන්ගේ එකතුවෙන් ප්රතික්රියකවල සම්මත ගිබ්ස් ශක්තීන්ගේ එකතුව අඩු කළ විට ප්රතික්රියාවේ සම්මත ගිබ්ස් ශක්ති විපර්යාසය ලැබේ.
විශේෂ කරුණු :
- ද්රව්යක සම්මත ගිබ්ස් ශක්තිය, එම ද්රව්ය උත්පාදනයට අදාල ප්රතික්රියාවේ සම්මත ගිබ්ස් ශක්ති විපර්යාසය ලෙස හැදින්වේ . එම නිසා සම්මත ගිබ්ස් ශක්තිය \triangle{G^\theta}_f ලෙසද සංකේතවත් කෙරේ.
- සම්මත අවස්ථාවේ පවතින මූලද්රව්යක සම්මත ගිබ්ස් ශක්තිය ශුන්ය බව සැලකේ .
- බහුරූපී ආකරයෙන් පවතින මූලද්රව්යවල වඩාත්ම සුලබම හෙවත් ස්ථායීම බහුරූපී ආකාරයේ සම්මත ගිබ්ස් ශක්තිය ශූන්ය වන බව සැලකේ.
- ප්රතික්රියාවක ∆Gᶿ හි අගය අනුව ප්රතික්රියාවේ ස්වයංසිද්ධතාවය (ඉබේම සිදුවීම) පුරෝකථනය කළ හැකිය.
පහත සදහන් පොදු ප්රතික්රියාව සලකමු.
A + B → C + D
- ∆Gᶿ = (-) නම්,
ප්රතික්රියාව ස්වයංසිද්ධව ඉදිරියට (→) සිදු වේ. එනම් A හා B මිශ්ර කල විට C හා D සෑදේ.A හා B වලින් සීමාකාරී ප්රතික්රියක අවසන් වන තුරුම C හා D සෑදේ.
- ∆Gᶿ = 0 නම්,
ප්රතික්රියාව සමතුලිතතාවයේ පවතී.එනම් A හා B මිශ්ර කළ විට ඒවාය්නෙ කොටසක් ප්රතික්ර්රිය කිරීමෙන් C හා D සෑදීමෙන් ද , C හා D මිශ්ර කල විට ඒවායෙන් කොටසක් ප්රතික්රියා කිරීමෙන් A හා B සෑදීමෙන්ද පද්ධතිය සමතුලිතතාවයට පත්වේ. සමතුලිතතාවය පහත සදහන් පරිදි සිදුවේ.
A + B ⇋ C + D
- ∆Gᶿ = (+) නම්,
ප්රතික්රියාව ස්වයංසිද්ධව ඉදිරියට සිදු නොවේ. නමුත් පසු අතට ප්රතික්රියාව ස්වයංසිද්ධ වේ. A හා B මිශ්ර කළ විට C හා D නොසෑදෙන නමුත් C හා D මිශ්ර කළ විට A හා B සෑදේ.
A + B → C + D X C + D → A + B √
- ප්රතික්රියාවක සම්මත ගිබ්ස් ශක්ති විපර්යාසය , සම්මත එන්තැල්පි විපර්යාසය සහ සම්මත එන්ට්රොපි විපර්යාසය අතර සම්බන්ධතාවය පහත පරිදි වේ.
මේ අනුව ප්රතික්රියාවක ස්වයංසිද්ධතාවය එහි ∆H , ∆S සහ නිරපේක්ශ උෂ්ණත්වය යන තුනෙහිම බලපෑමෙන් තීරණය වේ .
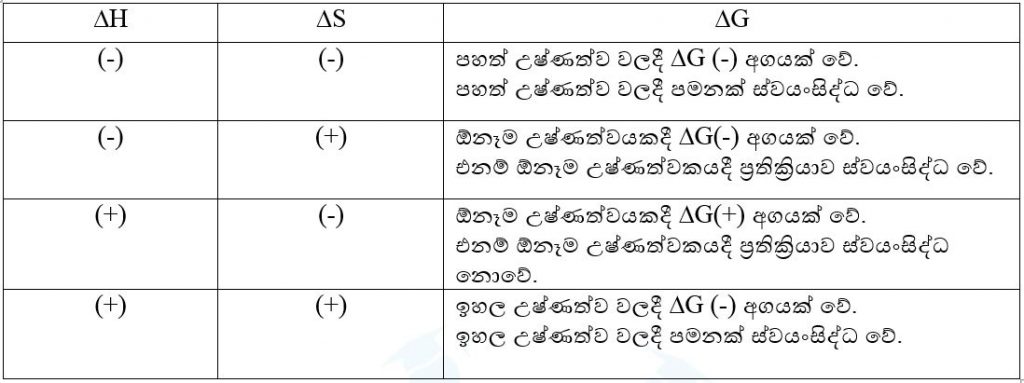
- පහත උදාහරණය සලකා බලමු.
(01) කාබන්ඩයොක්සයිඩ් හා හයිඩ්රජන් වායු මවුල එක බැගින් නියත පරිමා භාජනයක මිශ්ර කර 25 0C උෂ්ණත්වයක දී පහත පරිදි ප්රතික්රියා කිරීමට ඉඩ හරින ලදී.
CO2 (g) + H2 (g) → CO (g) + H2O (g)
25 0C ට අදාල තාප රසායනික දත්ත කිහිපයක් පහත වගුවේ දැක්වේ.

- 25 0C හිදී ඉහත ප්රතික්රියාවට අදාල ∆Gᶿ ගණනය කරන්න.
- 25 0C හිදී ඉහත ප්රතික්රියාවට අදාල ∆Sᶿ ගණනය කරන්න.
- එනයින් ඉහත ප්රතික්රියාව සදහා ∆Hᶿ ගණනය කරන්න .
- ඉහත ප්රතික්රියාව දී ඇති දිශාවට ස්වයංසිද්ධවේ ද ? ස්වයංසිද්ධ නොවන දිශාවට ප්රතික්රියාව ස්වයංසිද්ධව කරවීම සදහා කිසියම් T (K) උෂ්ණත්වයකට වඩා ඉහල උෂ්ණත්වයකට රත් කළ යුතු නම්, T හි අගය ගණනය කරන්න.
පිළිතුරු
01. ∆Gᶿ = ∑Gᶿඵල – ∑Gᶿප්රතික්රියක
= (-137-229) kJ mol-1 – (-394 – 0 ) kJ mol-1
= 28 kJ mol-1
02. ∆Sᶿ = ∑Sᶿඵල – ∑Sᶿප්රතික්රියක
= (197.5 + 188.7 ) JK-1mol-1 – ( 213.7 + 130.6 ) JK-1mol-1
= 41.9 JK-1mol-1
03. ∆Gᶿ = ∆Hᶿ – T∆Sᶿ
∆Hᶿ = ∆Gᶿ + T∆Sᶿ
= 28 kJ mol-1 + 298 K x 41.9 x 10-3 kJ K-1 mol-1
= 40.49 kJ mol-1
04. ∆Gᶿ > 0 බැවින් ප්රතික්රියාව දී ඇති දිශාවට ස්වයංසිද්ධ නොවේ. ස්වයංසිද්ධ වීම සදහා ∆G < 0 විය යුතුය .
∆H – T∆S < 0
\begin{array}{l}T\;>\;\frac{\triangle H}{\triangle S}\;=\;\frac{40.49\;\;kJmol^{-1}}{41.9\times10^{-3}\;kJK^{-1}mol^{-1}}\\\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\\\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;=\;966K\\\\\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;=693\;^0C\;\end{array}

