සංයුජතා කවචයට අවසානයට පිරෙන ඉලෙක්ට්රෝන p උපශක්ති මට්ටමට පිරෙන මූලද්රව්ය සමූහය p ගොනුවට අයත් වේ. 13,14,15,16,17,18 යන කාණ්ඩ p ගොනුවට අයත් වේ.
| 13 (ns2np1) | 14 (ns2np2) | 15 (ns2np3) | 16 (ns2np4) | 17 (ns2np5) | 18 (ns2np6) |
|---|---|---|---|---|---|
| He | |||||
| B | C | N | O | F | Ne |
| Al | Si | P | S | Cl | Ar |
| Ga | Ge | As | Se | Br | Kr |
| In | Sn | Sb | Te | I | Xe |
| Tl | Pb | Bi | Po | At | Rn |
A/L විෂය නිර්දේශයට අදාල p ගොනුව සම්බන්ධ න්යාය -1 කොටස
[youtube https://www.youtube.com/watch?v=3fpOSYw-dJ0]
A/L විෂය නිර්දේශයට අදාල p ගොනුව සම්බන්ධ න්යාය – 2 කොටස
[youtube https://www.youtube.com/watch?v=qC7o4ZODrac]
A/L විෂය නිර්දේශයට අදාල p ගොනුව සම්බන්ධ න්යාය – 3 කොටස
[youtube https://www.youtube.com/watch?v=bb0gELH3LZ8]
A/L විෂය නිර්දේශයට අදාල p ගොනුව සම්බන්ධ න්යාය – 4 කොටස
[youtube https://www.youtube.com/watch?v=HHi-ZXg2Kyk]
13 කාණ්ඩය (ns2np1)
- B (බෝරෝන්) ලෝහාලෝහයක් වන අතර B සංයෝග බොහෝමයක් සහසංයුජ වේ. B හි කුඩා පරමාණුක අරය නිසා අනෙක් සාමාජිකයන්ගෙන් වෙනස් වේ. B 14 කාණ්ඩයේ Si සමඟ ප්රබල විකර්ණ සම්බන්ධතාවක් පෙන්වයි.
- Al උභයගුණී ලක්ෂණ සහිත ලෝහයකි.
- Ga, In, Tl ලෝහ වේ.
- මෙම මූලද්රව්ය වලින් සෑදී ඇති සරල සංයෝගවල දී මූලද්රව්ය කිට්ටුම උච්ච වායු වින්යාසය ලැබී නැත. එම නිසා එම සංයෝගය එකසර ඉලෙක්ට්රෝන යුගල සහිත ප්රභේද සමඟ සංගත බන්ධන සාදා ගනියි.
Al – ඇලුමිනියම් – 1s22s22p63s23s23p1
- නිල් පාටට හුරු සුදු පැහැති සැහැල්ලු ශක්තිමත් ලෝහයකි.
- දීප්තිමත් පෘෂ්ඨයක් සහිතය.
- ඝනත්වය සාපේක්ෂව අඩුය.
- පෘථිවි කබොලෙහි 3 වෙනියට සුලභම මූලද්රව්ය සහ ස්කන්ධය අනුව වැඩිම ප්රතිශතයක් පවතින ලෝහය Al වේ.
- Al වල වාතයට නිරාවරණය වී ඇති පෘෂ්ඨිය O2 සමඟ ප්රතික්රියා කර Al2O3 ස්ථරයක් සෑදීම නිසා තවදුරටත් O2 සමඟ ප්රතික්රියා කිරීමට ප්රතිරෝධයක් ඇතිවේ. එම නිසා Al වාතය සමඟ ප්රතික්රියා නොකරන මූලද්රව්යක් ලෙස සැලකේ.
- Al වායුගෝලය තුළ රත් කල විට ඔක්සයිඩ හා නයිට්රයිඩ සාදයි.
\begin{array}{l}\circ\;4{\mathrm{Al}}_{(\mathrm s)}\;+\;3{\mathrm O}_{2(\mathrm g)}\;\rightarrow\;2{\mathrm{Al}}_2{\mathrm O}_{3(\mathrm s)\;}\\\circ\;2{\mathrm{Al}}_{(\mathrm s})\;+\;{\mathrm N}_{2(\mathrm g)}\;\rightarrow\;2{\mathrm{AlN}}_{(\mathrm s)}\end{array}
- මෙම ඵල මිශ්රණය ජලයට යෙදූ විට , NH3 නිදහස් වේ.
\circ\;{\mathrm{AlN}}_{(\mathrm s)\;}+\;3{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\;\rightarrow\;{\mathrm{NH}}_{3(\mathrm g)}\;+\;\mathrm{Al}(\mathrm{OH})_{3(\mathrm s)}
- Al උභයගුණී ලෝහයකි. අම්ල හා භෂ්ම සමඟ ප්රතික්රියා කර ලවණ හා H2 සාදයි.
\begin{array}{l}\circ\;2{\mathrm{Al}}_{(\mathrm s)}\;+\;6{\mathrm{HCl}}_{(\mathrm{aq})}\;\rightarrow\;2{\mathrm{AlCl}}_{3(\mathrm{aq})}\;+\;3{\mathrm H}_{2(\mathrm g)}\;\\\circ\;2{\mathrm H}_2{\mathrm O}_{(\mathrm l)\;}\;+\;2{\mathrm{Al}}_{(\mathrm s)}\;+\;2{\mathrm{NaOH}}_{(\mathrm{aq})}\;\rightarrow\;2{\mathrm{NaAlO}}_{2(\mathrm{aq})}\;+\;3{\mathrm H}_{2(\mathrm g)}\;\\\circ\;6{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\;\;+\;2{\mathrm{Al}}_{(\mathrm s)}\;+\;2{\mathrm{NaOH}}_{(\mathrm{aq})}\;\rightarrow\;2\mathrm{NaAl}(\mathrm{OH})_{4(\mathrm{aq})}\;+\;3{\mathrm H}_{2(\mathrm g)}\end{array}
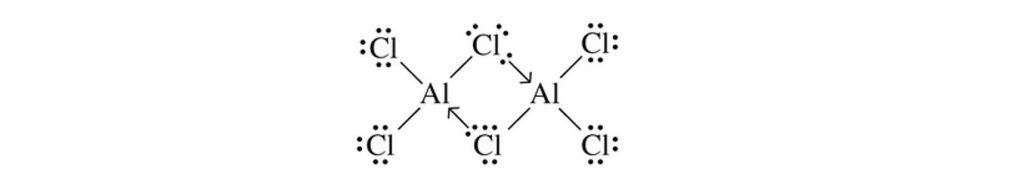
- AlCl3 සංයෝගයේ අෂ්ඨකය සම්පූර්ණ වී නොමැති නිසා වායු අවස්ථාවේදී මෙය Al2Cl6 ලෙස ද්විඅවයවයක් ලෙස පවතී.
- Al3+ අයන ජලීය ද්රාවණයක දී පවතින්නෙ ජල අණු 6 ක් සමඟ බැදී සංකීර්ණ සංයෝගයක් ලෙසයි. Al3+ අයනයේ ඉහළ ධන අරෝපණය සහ කැටායනික අරය අඩු වීමත් නිසා එහි ඇති ඉහළ ධ්රැවීකරණ බලය හේතුවෙන් මෙම සංකීර්ණය ජල විච්ඡේදනය වී මාධ්ය ආම්ලික කරයි.
\circ\;6{\mathrm H}_2{\mathrm O}_{(\mathrm{aq})}\;+\;{\mathrm{Al}^{3+}}_{(\mathrm{aq})}\rightarrow\;\lbrack\mathrm{Al}({\mathrm H}_2\mathrm O)_6{\rbrack^{3+}}_{(\mathrm{aq})}

\circ\;{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\;+\;\lbrack\mathrm{Al}({\mathrm H}_2\mathrm O)_5(\mathrm{OH})\rbrack^{2+}\;\rightarrow\;\lbrack\mathrm{Al}({\mathrm H}_2\mathrm O)_4(\mathrm{OH})_2\rbrack^+\;+\;{\mathrm H}_3\mathrm O\;^+
- මෙම ආම්ලික මාධ්යයට NaOH භෂ්ම බිංදු කිහිපයක් යෙදීමේදී OH¯ අයන ආකලනය වී, සුදු ජෙලටිනිමය Al(OH)3 නිපදවයි.
- මෙම අවක්ෂේපය අතිරික්ත OH¯ අයන (ප්රබල භෂ්මයක්) සමඟ [Al(OH)4]¯ (ටෙට්රාහයිඩ්රොක්සයිඩෝ ඇලුමිනේට්) සංකීර්ණ අයන බවට පත් වී ද්රාවණ ගත වී අවර්ණ ද්රාවණයක් සාදයි.
- එයට නැවත HCl යෙදූ විට නැවත සුදු අවක්ෂේපය ලැබේ.එම අවක්ෂේපයට නැවත HCl යෙදූ විට නැවත අවර්ණ ද්රාවණය ලැබේ.


