14 කාණ්ඩය
- ns2np2 ඉලෙක්ට්රෝන වින්යාසයට අයත් මූල ද්රව්ය මෙයට අයත් වේ.
- මෙම කාණ්ඩයේ C අලෝහයක් වේ. Ge සහ Si ලෝහාලෝහ වේ. Sn, Pb ලෝහ වේ. ඒවාගේම Sn හා Pb උභයගුණී ලක්ෂණ පෙන්වයි.
- සහසංයුජ බන්ධන ජාල ව්යුහයක් පෙන්වීම හේතුවෙන් 14 කාණ්ඩයේ පළමු මූලද්රව්ය 3 සතුව ඉහළ ද්රවාංක පවතියි.
- Si සහ Ge අර්ධ සන්නායක කර්මාන්තයේදී ප්රධාන වශයෙන් භාවිත කෙරේ.
- කාණ්ඩයේ පහළට යත්ම +4 ඔක්සිකරණ තත්වයේ ස්ථායීතාවය අඩුවී +2 ඔක්සිකරණ තත්වයේ ස්ථායීතාවය වැඩිවේ.
C – කාබන් – 1s22s22p2
- ප්රධාන සංයුජතාවය 4 කි.
- නිදහස් ධන හෝ ඍණ අයන නොසාදයි.
- අලෝහයක් වුවත් විද්යුත් සන්නායක හැකියාව පවතියි.
- C වල ඉලෙක්ට්රොනික වින්යාසය අනුව +4 සිට -4 දක්වා ඔක්සිකරණ අංක පෙන්වයි. ඊට අමතරව +4 සිට -4 දක්වා සියළු සංයෝග සෑදිය හැක.
| +4 | +3 | +2 | +1 | 0 | -1 | -2 | -3 | -4 |
| CO2 | C2Cl6 | CO | H2C2Cl4 | H2CO | C2H2 | C2H4 | C2H6 | CH4 |
- සාන්ද්ර අම්ල හමුවේ ඔක්සිකරණය වේ.
\begin{array}{l}\circ\;\mathrm C\;+\;4{\mathrm{HNO}}_3\;\rightarrow\;2{\mathrm H}_2\mathrm O\;+\;4{\mathrm{NO}}_2\;+\;{\mathrm{CO}}_{2\;}\\\circ\;\mathrm C\;+\;{\mathrm H}_2{\mathrm{SO}}_4\;\rightarrow\;{\mathrm{CO}}_2\;+\;{\mathrm H}_2\mathrm O\;+\;{\mathrm{SO}}_2\end{array}
- එකම භෞතික තත්වය යටතේ දී එකම මූලද්රව්යයේ අණු හෝ පරමාණු සැකැස්ම වෙනස් වීම නිසා එකිනෙකට වෙනස් ගති ලක්ෂණ පෙන්වීම බහුරූපිතාවය ලෙස හැදින්වේ.
- C වල ස්ඵටිකරූපී හා අස්ඵටිකරූපී ලෙස බහුරූපී ආකාර 02 කි.
|
ස්ඵටිකරූපී |
අස්ඵටිකරූපී |
|
දියමන්ති |
ගල් අඟුරු |
|
මිනිරන් |
කෝක් (Coke) |
|
ෆුලරින් |
|
|
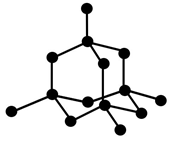
දියමන්ති |
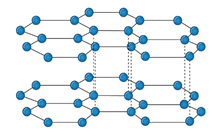
මිනිරන් |
 |
 |
|
ත්රිමාණ සහසංයුජ දැලිසකි. |
ද්විමාන පැතලි ස්ථර ලෙස පවතී. ස්ථර අතර දුබල ලන්ඩන් බල පවතී. |
|
එක් C පරමාණුවක් තවත් C පරමාණු 4 කට චතුස්තලිකව බැඳීමෙන් දැලිස සෑදී ඇත. |
එක් C පරමාණුවක් තවත් C පරමාණු 3 ක් සමඟ තලීය ත්රිකෝණාකාරව බැදී C සඩාස්ර නිර්මාණය වී ඇත. |
|
sp3 මුහුම්කරණය දක්වයි. |
sp2 මුහුම්කරණය දක්වයි. |
|
දෘඪතාවය ඉතා ඉහළයි. |
දෘඪතාවය සාපේක්ෂව අඩුය. |
|
ද්රවාංකය සාපේක්ෂව ඉහළයි. |
ද්රවාංකය සාපේක්ෂව ඉහළ අගයක් ගනී. |
|
තාපාංක එකිනෙක සමානයි. |
තාපාංක එකිනෙකට සමාන වේ. |
|
ආලෝකය විනිවිද යයි. |
ආලෝකය විනිවිද නොයයි. |
|
භාවිත : වීදුරු කැපීම ආභරණ සෑදීම |
ස්ථර අතර පවතින නිදහස් ඉලෙක්ට්රෝන වලාව නිසා විද්යුත් හා තාප සන්නායක ගුණ ඇත. |
|
|
ස්ථර අතර පවතින දුබල අපකිරණ බල නිසා ස්ථර එකිනෙක මත ලිස්සා යාමේ හැකියාව ඇත. එම නිසා ලිහිසි ගුණ ඇත. |
|
|
භාවිත : ඉලෙක්ට්රෝඩ සෑදීමට යොදා ගනී. පැන්සල් සෑදීමට යොදාගනී. |
CO – කාබන් මොනොක්සයිඩC වල ඔක්සයිඩ
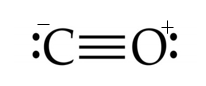
- මෙතනොයික් හෝ ඔක්සලික් අම්ලය සාන්ද්ර H2SO4 අම්ලය සමඟ රත් කිරීමෙන් නිෂ්පාදනය කෙරේ.
\begin{array}{l}\circ\;{\mathrm{HCOOH}}_{(\mathrm l)}\xrightarrow[\triangle]{\mathrm{සා}.{\mathrm H}_2{{\mathrm{SO}}_4}_{(\mathrm{aq})}}{\mathrm{CO}}_{(\mathrm g)}+3{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\\\circ\;{\mathrm H}_2{\mathrm C}_2{\mathrm O}_{4(\mathrm s)}\xrightarrow[\triangle]{\mathrm{සා}.{\mathrm H}_2{{\mathrm{SO}}_4}_{(\mathrm{aq})}}{\mathrm{CO}}_{(\mathrm g)}+{\mathrm{CO}}_{2(\mathrm g)}+3{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\end{array}
- අවර්ණ, අගන්ධ, උදාසීන විශ වායුවකි.
- CO නිල් පැහැ දැල්ලකින් වාතයේ දැවී CO2 සාදයි.
- යකඩ නිස්සාරණයේදී ඔක්සිහාරකයක් ලෙස සුලභව භාවිතා වේ.
\circ\;{\mathrm{Fe}}_2{\mathrm O}_{3(\mathrm s)}\;+\;3{\mathrm{CO}}_{(\mathrm g)}\;\xrightarrow\triangle2{\mathrm{Fe}}_{(\mathrm s)}\;+\;3{\mathrm{CO}}_{2(\mathrm g)}
- කාර්මික ඉන්ධනයක් ලෙස භාවිත වේ.
CO2 – කාබන් ඩයොක්සයිඩ්
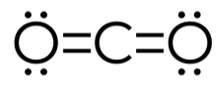
- CO වායුව වාතයේ දහනයෙන් CO2 වායුව සෑදේ.
\begin{array}{l}\circ\;2{\mathrm{CO}}_{(\mathrm g)}\;+{\mathrm O}_{2(\mathrm g)}\;\;\rightarrow\;2{\mathrm{CO}}_{2(\mathrm g)\;}\\\circ\;{\mathrm{CaCO}}_{3(\mathrm s)}\;+\;2{\mathrm{HCl}}_{(\mathrm{aq})}\;\rightarrow\;{\mathrm{CaCl}}_{2(\mathrm{aq})}\;+\;{\mathrm{CO}}_{2(\mathrm g)}+\;{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\end{array}
- අවර්ණ, අගන්ධ, දුබල ආම්ලික වායුවකි.
\circ\;{\mathrm{CO}}_{2(\mathrm g)}\;+\;2{\mathrm{NaOH}}_{(\mathrm{aq})}\;\rightarrow\;{\mathrm{Na}}_2{\mathrm{CO}}_{3(\mathrm{aq})}\;+\;{\mathrm H}_2{\mathrm O}_{(\mathrm l)}
- CO2 අණු අපකිරණ බන්ධන වලින් බැඳී ඝන වූ විට එය වියළි අයිස් ලෙස හැඳින්වේ. වියළි අයිස් අධි ශිතකාරකයක් සහ කෘතිම වැසි ඇති කිරීමට භාවිත කරයි.
- CO2 වායුව Na2CO3 නිෂ්පාදනයට, ගිනි නිවන උපකරණ සඳහා ද යොදා ගැනේ.
- CO2 වායුව ජලයේ දියවී දුබල ද්විභාෂ්මික කාබනික (H2CO3) අම්ලය සාදයි.
\begin{array}{l}\circ\;{\mathrm{CO}}_{2(\mathrm g)}\;+\;{\mathrm H}_2{\mathrm O}_{(\mathrm l)}\;\;\leftrightharpoons\;{\mathrm H}_2{\mathrm{CO}}_{3(\mathrm{aq})}\;\\\circ\;{\mathrm H}_2{\mathrm{CO}}_{3(\mathrm{aq})}\;\leftrightharpoons\;{\mathrm{HCO}_3^-}_{(\mathrm{aq})}\;+{\mathrm H^+}_{(\mathrm{aq})}\;\\\circ\;{\mathrm{HCO}_3^-}_{(\mathrm{aq})}\;\leftrightharpoons\;{\mathrm{CO}_3^{2-}}_{(\mathrm{aq})}\;+\;{\mathrm H^+}_{(\mathrm{aq})}\end{array}
- උෂ්ණත්වය ඉහළ ගියහොත් H2CO3 වියෝජනය වෙමින් CO2 හා ජලය සාදයි.
- CO2 හුණු දියර (Ca(OH)2) තුළට යෙදූ විට සුදු අවක්ෂේපයක් සෑදී ,වැඩිපුර CO2 වායු බූබුළනයේදී සුදු අවක්ෂේපය දියවී අවර්ණ ජලීය ද්රාවණයක් ලැබේ (Ca(HCO3)2).

