ප්රබල විද්යුත් විච්ඡේද්ය
- ජලයේ දී සම්පූර්ණයෙන්ම අයන වලට වෙන් වේ.
උදා : ප්රබල අම්ල – HCl , HNO3 , H2SO4
ප්රබල භෂ්ම – NaOH , Ba(OH)
ද්රාව්ය ලවණ – NH4Cl , KCl
- ලවණ සේතුව සදහා ප්රබල විද්යුත් විච්ඡේද්යක් භාවිත කළ යුතු අතර මේ සදහා ප්රබල අම්ල හෝ ප්රබල භෂ්ම භාවිත නොකෙරේ.
දුබල විද්යුත් විච්ඡේද්ය
- ජලයේ දී සම්පූර්ණයෙන් අයන වලට වෙන් නොවේ.
උදා : දුබල අම්ල
දුබල භෂ්ම
H2O
විද්යුත් අවිච්ඡේද්ය
- අයන අඩංගු නොවන ද්රවමය සංයෝග
උදා : C6H6 , C7H16
- මේවා විද්යුතය සන්නයනය නොකරයි.
ද්රාවණයක සන්නායකතාවය කෙරෙහි බලපාන සාධක
- ද්රාවණයේ ස්වභාවය (ප්රබල / දුබල විද්යුත් විච්ඡේද්ය / විද්යුත් අවිච්ඡේද්ය)
- ද්රාවණයේ සාන්ද්රණය
- උෂ්ණත්වය
සාන්ද්රණය
- තනුක ජලීය ද්රාවණයක සාන්ද්රණය අඩු කරන විට ඒ සමග සන්නායකතාවද අඩුවේ.
- මීට හේතු වන්නේ තනුක කිරීමේදී ද්රාවනයේ අයන අතර ඇති අන්තර් ක්රියා ප්රමානය අඩු වීමයි.
| නියැදිය |
සන්නායකතාව / µS cm-1 |
| ආසැත ජලය | 1-2 |
| 0.01mol dm-3 KCl ද්රාවණය | 1,480 |
| 0.10 mol dm-3 KCl ද්රාවණය | 12,400 |
| 1.0 mol dm-3 KCl ද්රාවණය | 110,000 |
| ළිං ජලය | 100-200 |
| නල ජලය | 50-150 |
| මුහුදු ජලය | 40,000 |
උෂ්ණත්වය
- ද්රාවණයක උෂ්ණත්වය වැඩි කරන විට අයන වල වේගය වැඩි වන බැවින් දෙන ලද සාන්ද්රණයක් ඇති ද්රාවණයක වැඩි කිරීමට එය හේතු වේ.
| සාන්ද්රණය | සන්නායකතාව /µS cm-1 | ||
| 0°C | 13°C | 25°C | |
| 1.00 KCl ද්රාවණය | 6.5×104 | 9.8×104 | 1.1×105 |
| 0.10 KCl ද්රාවණය | 7.2×103 | 1.1×104 | 1.3×104 |
| 0.01 KCl ද්රාවණය | 7.8×102 | 1.2×103 | 1.4×103 |
ද්රාව්යයේ ස්වභාවය
-
-
- සෑදෙන අයන හෝ ආරෝපණ වාහක ප්රමානය, ද්රාව්යයේ ස්වභාවය මගින් තීරණය වේ.
- ප්රභල විද්යුත් විච්චේද්ය, ජලිය ද්රාවණයේදී පූර්ණව අයන බවට විඝටනය වන බැවින් ඒවාට විද්යුතය සන්නයනය කල හැකිය.
- කෙසේ වුවද, මෙම ප්රබල විද්යුත් විච්චේද්ය වල ඝන අවස්ථාවේදී සචල අයන නැති නිසා, ඝන අවස්ථාවේදී විද්යුතය සන්නයනය නොකරයි.
- නමුත් ඒවා විලීන අවස්ථාවට ප්ත් කලහොත් අයනවලට යම් සචලතාවක් ලැබෙන බැවින් විද්යුතය සන්නයනය කල හැකිය.
-
(උදා – NaCl, KCl)
-
-
- දුබල අම්ල හා දුබල භෂ්ම ජලයේදී භාගිකව අයණීකරණය වුවත් එහිදී අයන සෑදෙන බැවින් විද්යුතය සන්නයනය කල හැකිය.
-
මේ සියලු සාධක සන්නායකතාව කෙරෙහි බලපාන්නේ ආරෝපණ වාහක වල සචලතාව, මේ සාධක මත රදා පවතින බැවිනි.
-
- දෙන ලද උෂ්ණත්වයකදී හා දෙන ලද විද්යුත් ක්ෂේත්රයකදී, යම් අයනයක් මගින් ගෙන යන ධරාව, අයන වල සාන්ද්රණය හා ඒවායේ වේගය මත රදා පවතී.
- අයනයක වේගය එහි ආරෝපණ ප්රමාණය හා සපයන ලද විද්යුත් ක්ෂේත්රයේ විභව අනුක්රමණය මත රදා පවතී.
- ජල නියැදියක් ඇති අයන අන්තර්ගතය විශ්ලේෂණය කිරීමේදී ද්රාවණයක සන්නායකතාව ඉතා වැදගත් වේ.
- ප්රායෝගිකව ද්රාවණයක සන්නායකතාව මනින්නේ සන්නායකතාමීටරය මගිනි.
- මේ මිනුම් ලවණතාව ප්රමානනය කිරීමට, ද්රාව්යතා ගුණිතය ගණනය කිරීම හා වෙනත් විවිධ භාවිත සදහා යොදා ගනී.
- ජලීය ද්රාවණ වල දී H+ හා OH– වලට උපරිම වේගයක් ඇති නිසා එම අයන සන්නායකතාවය සඳහා වැඩිපුර ම බලපායි.
- තනුක ජලීය ද්රාවණ වලදී H+ අයන වලට උපරිම වේගයක් ඇති නිසා සන්නායකතාවයෙන් 80% පමණ සිදුවනුයේ H+ අයන මගිනි.
ඉලෙක්ට්රෝඩය
සංයුජතාවය n වන ලෝහයක් එම ලෝහයේම අයන ද්රාවණයක් තුල ලෝහය ගිල්වා ඇති අවස්ථාව සලකමු.
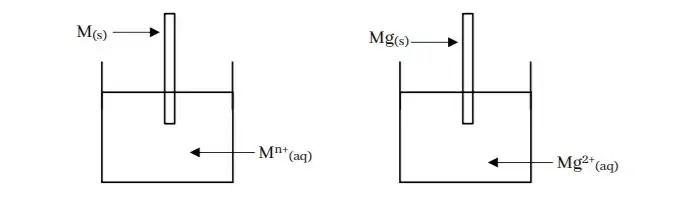
- ලෝහයෙහි ඇති පරමාණු ඔක්සිකරණය වී ඉලෙක්ට්රෝන ලෝහ තහඩුවෙහි රදවමින් අයන ද්රාවණගත වේ.
\begin{array}{l}{\mathrm M}_{(\mathrm s)}\;\rightarrow\;{\mathrm M^{\mathrm n+}}_{(\mathrm{aq})}\;+\;\mathrm n\;\mathrm e\\{\mathrm{Mg}}_{(\mathrm s)}\;\rightarrow\;{\mathrm{Mg}^{2+}}_{(\mathrm{aq})}\;+\;2\;\mathrm e\\\end{array}
- ද්රාවණයෙහි ඇති අයන ලෝහයෙන් ඉලෙක්ට්රෝන ලබා ගනිමින් (ඔක්සිකරණය වී) ලෝහ පරමාණු ලෙස තහඩුවෙහි රැදේ.
\begin{array}{l}\;{\mathrm M^{\mathrm n+}}_{(\mathrm{aq})\;\;}\;+\mathrm n\;\mathrm e\;\;\rightarrow{\mathrm M}_{(\mathrm s)}\\\;{\mathrm{Mg}^{2+}}_{(\mathrm{aq})}\;+\;2\;\mathrm e\rightarrow{\mathrm{Mg}}_{(\mathrm s)}\\\end{array}
- කිසියම් මොහොතකදී ඉහත ක්රියාවලි 2 හි සීඝ්රතා සමාන වී ගතික සමතුලිතතාවයක් ඇති වේ.
\begin{array}{l}{\mathrm M}_{(\mathrm s)}\;\;\;\rightleftharpoons\;{\mathrm M^{\mathrm n+}}_{(\mathrm{aq})}\;+\;\mathrm n\;\mathrm e\\{\mathrm{Mg}}_{(\mathrm s)}\;\rightleftharpoons\;{\mathrm{Mg}^{2+}}_{(\mathrm{aq})}\;+\;2\;\mathrm e\\\end{array}
- මෙලෙස ඔක්සිකරනයක් හා ඔක්සිහරනයක් සිදුවිය හැකි පද්ධතියක් ඉලෙක්ට්රෝඩයක් ලෙස හැදින්විය හැක.
- ඉලෙක්ට්රෝඩය මත දී ගතික සමතුලිතයක් හට ගනී.
- ඉලෙක්ට්රෝඩයක සමතුලිත ක්රියාව ලිවීමේ දී ඉදිරි ක්රියාව ඔක්සිකරණයක් වන පරිදි ලිවීම සම්මතය වේ.

