පදාර්ථය යනු විශ්වයේ ඉඩක් ගන්නා සහ ස්කන්ධයක් සහිත භෞතික ද්රවය්යකි.
පරමාණුව – සියලු පදාර්ථ නිර්මාණය වී ඇත්තේ පරමාණු වලිනි.දෙන ලද මුලද්රව්යකට ආවේණික ගුණ පෙන්වන ඉතා කුඩා අංශුව එම මූලද්රව්යයේ පරමාණුව වේ.
පරමාණුවේ පැවැත්ම,
- x කිරණ විවර්තනයෙන්
- ස්කන්ධ වර්ණාවලි මගින්
- ක්ෂේත්ර අයනීකරණ අන්වීක්ෂ මගින් දැනගත හැක.
පරමාණුව යන පදයට පළමුවෙන්ම සාර්ථක පැහැදිලිකිරීමක් ඉදිරිපත් කලේ ජෝන් ඩෝල්ටන් ය.
ඩෝල්ටන්ගේ පරමාණුක වාදයේ උපකල්පන
1.මූලද්රව්ය සෑදී ඇත්තේ ‘පරමාණු’ යනුවෙන් හැඳින්වෙන, අතිශයින්ම කුඩා , බෙදිය නොහැකි අශුවලිනි.
2.යම් මූලද්රව්යක සියලු පරමාණු ස්කන්ධයෙන් හා තරමින් එකිනෙකට සමාන වන අතර යම් මූලද්රව්යක පරමාණු අන් සියලු මූලද්රව්යවල පරමාණුවලින් වෙනස් වේ.
3.රසායනික ප්රතික්රියාවලින් එක් මූලද්රව්යක පරමාණු , තවත් මූලද්රව්යක පරමාණු බවට වෙනස් කළ නොහැකිය.එනම් රසායනික ප්රතික්රියාවලදී පරමාණු මැවීමට හෝ විනාශ වීමට භාජනය නොවේ.
4.වෙන් වෙන් මූලද්රව්යවල පරමාණු දෙකක් හෝ වැඩි ගණනක් සරල සංඛ්යාත්මක අනුපාතවලින් සම්බන්ධ වීමෙන් සංයෝග ඇති වේ.
ඩෝල්ටන්ගේ පරමාණුක ආකෘතිය හැඳින්වෙන්නේ ‘ගොල්ෆ් බෝල ආකෘතිය’ යනුවෙනි.
පරමාණුකවාදයට අද හිමි තත්ත්වය
- පරමාණුව තුල ඉලෙක්ට්රෝන,ප්රෝටෝන,නියුට්රෝන ආදී උපපරමාණුක අංශු ඇත.
- න්යෂ්ටික ප්රතික්රියාවන් මගින් හා විකිරණශීලීතාවයේ දි පරමාණු බීදීම හා නව පරමාණු සෑදීම සිදුවේ.
- පරමාණු මැවීම හා නැසීම සිදුකල හැකිය යන මතය බිදවැටේ.
- සමස්ථානික සොයාගැනීම
- එකම මූලද්රව්යයේ පරමාණු සමාන නොවන බව තහවුරු වීම.
- එකම මූලද්රව්යයේ පරමාණු සමාන බව හා වෙනස් මූලද්රව්ය වල පරමාණු වෙනස් වේ යන මතය බිදවැටේ.
ඩෝල්ටන්ගේ පරමාණුකවාදයෙන් පදාර්ථයේ අංශුමය ස්වභාවය පිලිබද ඉතා වැදගත් අදහස් පල කලත් පදාර්ථයේ සිදුවන විපර්යාස පිලිබද විස්තර කිරිමකට හෝ පදාර්ථයේ විද්යුත් ස්වභාවය පිලිබද විස්තර කිරීමක් සිදු නොවීය.පරමාණුව උප පරමාණුක අංශුවලින් සමන්විත බව පැහැදිලි කිරීමට පදාර්ථයේ විද්යුත් ස්වභාවය යොදාගනී.
පදාර්ථයේ විද්යුත් ස්වභාවය සදහා සාක්ෂි
විද්යුත් ස්වභාවය යනු යම් පරමාණුවක පවතින ප්රෝටෝන ගණනට වඩා ඉලෙක්ට්රෝන ගණන වෙනස් වීමයි.
සාක්ෂි,
1.ඝර්ෂණය හෙවත් ස්ථිති විද්යුතය මගින් ලැබෙන සාක්ෂි.
- වීදූරු දණ්ඩක් සේදරෙදි කැබැල්ලකින් පිරිමැද්ද විට දණ්ඩ ධනව ආරෝපණය වීම.එනම් පදාර්ථයේ විද්යුතමය ස්වභාවයක් ඇත.
2.විද්යුත් විච්ඡේදනයෙන් ලැබෙන සාක්ෂි.
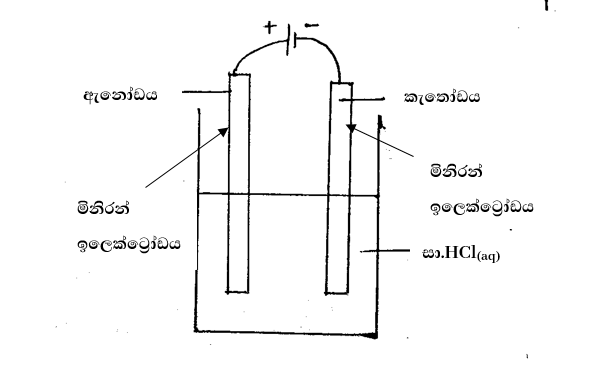
\begin{array}{l}\mathrm{Cathod}\Rightarrow\;2\mathrm H^++2\mathrm e\rightarrow\;{\mathrm H}_2\\\mathrm{Anod}\;\Rightarrow2\mathrm{Cl}^-\rightarrow\;{\mathrm{Cl}}_2+2\mathrm e\end{array}
- එනම් පදාර්ථයේ ද්රව අවස්ථාව ඉලෙක්ට්රෝන මගින් වායු අවස්ථාව බවට පත්කල හැක.
3.සරල කෝෂ මගින්(පදාර්ථ වල සිදුවන වෙනස් වීම් ආශ්රිතව විද්යුතය ජනනය වීම)
තනුක සල්ෆියුරික් ද්රාවණයකට Zn හා Ca තහඩු දමා ඒවා ද්රාවණ තුලදි හෝ පිටතදී එකිනෙක ස්පර්ශ නොවනසේ සකසා කුඩා බල්බයක් සවිකල විට බල්බය දැල්වේ.
බල්බය හරහා ඉලෙක්ට්රෝන ධාරාවක් ගමන් කරන බව පෙනේ.
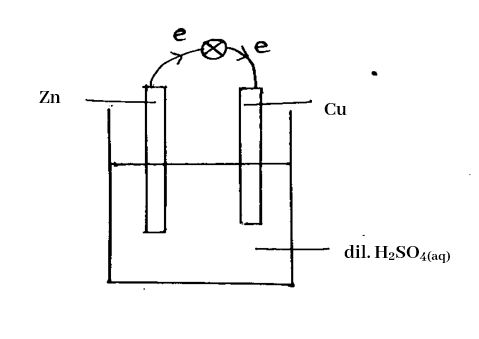
\text{Cu ඉලෙක්ට්රෝඩය මත}\;\\2\mathrm H^+{(\mathrm{aq})\;}+\;2\mathrm e\;\rightarrow\;\mathrm H{2(\mathrm g)}\\\text{ Zn ඉලෙක්ට්රෝඩය මත}\;\\\mathrm{Zn}{(\mathrm s)}\;\rightarrow{\mathrm{Zn}^{2+}}_{(\mathrm{aq})}+\;2\mathrm e
නිරීක්ෂණ ;-
- Cu අසලින් වායු බුබුළු පිට වේ.
- Zn තහඩුව දිය වේ.
පදාර්ථයේ ඝන, ද්රව, වායු අවස්ථාවල විද්යුත් ස්වභාවය පැහැදිලි කිරීමට උදාහරණ
- ඝන අවස්ථාව – ස්ථිති විද්යුතයෙන් ලැබෙන සාක්ෂි
- ද්රව අවස්ථාව – විද්යුත් විච්ඡේදනයෙන් ලැබෙන සාක්ෂි
- වායු අවස්ථාව – කැතෝඩ කිරණ පරීක්ෂාව
වැඩිදුර අධ්යනයට ,

