පද්ධතිය,වටපිටාව හා සීමාව
- තාප රසායනය යනු රසායන විද්යා අධ්යයන ක්ෂේත්රයේ දීර්ඝ ඉතිහාසයක් ඇති විෂය පථයකි. අප තාප රසායනය යනුවෙන් හඳුන්වන්නේ රසායනික ප්රතික්රියාවල දී සිදුවන තාප ශක්ති හුවමාරුව පිළිබඳ අධ්යයනයයි.
පද්ධතිය :-
- විශ්වයේ අපගේ සැලකිල්ලට භාජනය වන යම් කොටසක් වේද, එය පද්ධතියක් ලෙස හැඳින්වේ.
- උදා : පරීක්ෂණ සඳහා යොදාගත් ප්ලාස්කුව , කැලරි මීටරය ,…..
පරිසරය/වටපිටාව :-
- පද්ධතිය හැරුණු විට විශ්වයේ අන් සියලුම දෑ පරිසරයට අයත් වේ.
මායිම/සීමාව :-
- පද්ධතිය පරිසරයෙන් වෙන් කරනු ලබන්නේ මායිමෙනි.
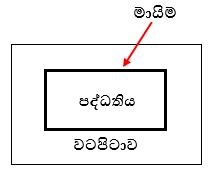
පද්ධති වර්ග
- පද්ධති හා වටපිටාව අතර සිදුවන විවිධාකාර අන්තර්ක්රියා/ක්රියාවලි අනුව ආකාර කිහිපයක පද්ධති අර්ථ දැක්විය හැකිය.
- විවෘත පද්ධති
- සංවෘත පද්ධති
- ඒකලිත පද්ධති
- සමජාතීය පද්ධති හා විෂමජාතීය පද්ධති
1.විවෘත පද්ධති :-
- පද්ධතිය හා පරිසරය අතර පදාර්ථය හා ශක්තිය යන දෙකම මායිම හරහා හුවමාරුවන පද්ධති විවෘත පද්ධති ලෙස හැඳින්වේ.

2.සංවෘත පද්ධති :-
- පද්ධතිය හා පරිසරය අතර පදාර්ථය හුවමාරු නොවී මායිම හරහා ශක්තිය පමණක් හුවමාරු වන පද්ධති සංවෘත පද්ධති ලෙස හැඳින්වේ.

3.ඒකලිත පද්ධති :-
- කිසියම් පද්ධතියක මායිම හරහා පදාර්ථය හෝ ශක්තිය හෝ යන දෙකෙන් එකක්වත් සංක්රමණය නොවන්නේ නම් එබඳු පද්ධතියක් ඒකලිත පද්ධතියක් ලෙස හැඳින්වේ.

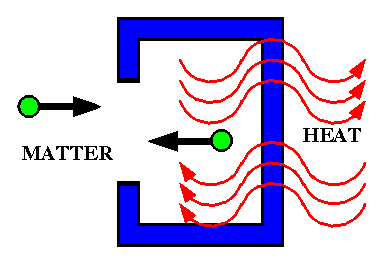
විවෘත පද්ධති
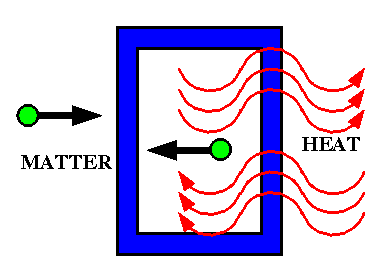
සංවෘත පද්ධති
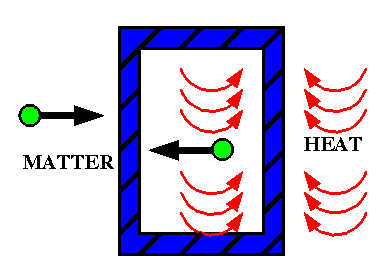
ඒකලිත පද්ධති
4.සමජාතීය පද්ධති හා විෂමජාතීය පද්ධති:-
- පද්ධතියක අඩංගු සියලු පදාර්ථ වල භෞතික අවස්ථාව ඒකාකාර වේ නම් එවැන්නකට සමජාතීය පද්ධතියක් යැයි කියනු ලැබේ.
- පද්ධතිය අඩංගු සියලු පදාර්ථ /සංඝටක වල භෞතික අවස්ථාව ඒකාකාර නොවේ නම් එවැන්නකට විෂමජාතීය පද්ධතියක් යැයි කියනු ලැබේ.
පද්ධතියක ගුණ
1.අන්වීක්ෂීය ගුණ
- පද්ධතියක් පරමාණුක හෝ අණුක පරිමාණයක ඇත්නම් එය අන්වීක්ෂීය පද්ධතියකි. එනම් සංවෘත බඳුනක් වැනි කිසියම් පද්ධතියක ඇතුළත් පරමාණුවල /අණුවල චාලක ශක්තිය,වේගය වැනි පරමාණුක හෝ අණුක පරිමාණ ඇසුරෙන් වක්ර ක්රම භාවිතයට ගනිමින් නිර්ණය කළ යුතු ගුණ අන්වීක්ෂීය ගුණ වේ.
2.මහේක්ෂ ගුණ
- පද්ධතියක සමස්ත හෝ මහේක්ෂ ගුණ අවස්ථාව හා අනුබද්ධ ගුණ මහේක්ෂ ගුණ නම් වේ .
පද්ධතියක ඇති මහේක්ෂ ගුණ තවදුරටත් වර්ග දෙකකට බෙදිය හැකිය.
Ⅰ.විත්ති ගුණ :-
-
-
-
- ද්රව්ය ප්රමාණය මත රඳා පවතින ගුණ විත්ති ගුණ ලෙස හැඳින්වේ . ස්කන්ධය,පරිමාව,ද්රව්ය ප්රමාණය විත්ති ගුණ වලට නිදසුන් වේ.
-
-
Ⅱ.ඝටනා ගුණ :-
-
-
-
- ද්රව්යයේ ප්රමාණය මත රඳා නොපවතින ගුණ ඝටනා ගුණ ලෙස හැඳින්වේ. උෂ්ණත්වය,ඝනත්වය, වර්තනාංකය, දුස්රාවීතාවය, පීඩනය, මවුලික ස්කන්ධය,මවුලික පරිමාව ඝටනා ගුණ වලට නිදසුන් වේ.
-
-
පද්ධතියක අවස්ථාව
පද්ධතියක අවස්ථාව පද්ධතියේ සුවිශේෂීව මැනිය හැකි මහේක්ෂීය ගුණ මගින් අර්ථ දැක්වේ.
1.ආරම්භක අවස්ථාව :-
- පද්ධතිය වටපිටාව සමඟ කොයි යම් හෝ ආකාරයේ අන්තර් ක්රියාවක් සිදු කිරීමට පෙර පද්ධතිය අනුබද්ධ මුල් අවස්ථාවයි.
2.අවසන් අවස්ථාව :-
- පද්ධතිය වටපිටාව හා සිදුකරන අන්තර් ක්රියාවලින් පසු එළඹෙන අවස්ථාවයි.
මීට අමතරව,
අවස්ථා ශ්රිතය:
-
- අවස්ථාව නිශ්චය කරගැනීම සඳහා යොදාගන්නා කිසියම් මහේක්ෂ ගුණයක් අවස්ථා ශ්රිතයක් ලෙස හඳුන්වයි.
-
- අවස්ථා ශ්රිතයක් එක් අගයක සිට වෙනත් අගයකට වෙනස් වුවහොත් එය ශ්රිත විපර්යාසයකි. ශ්රිත විපර්යාසය ගණනය කළ යුත්තේ සෑම විටම පසු අගයෙන් පෙර අගයයි.
සම්මත අවස්ථාව:
-
- IUPAC සම්මතය අනුව තාපය හා ශක්තිය සම්බන්ධ ගණනය කිරීම්වලදී සම්මත උෂ්ණත්වය 250C / 298K ද, සම්මත පීඩනය 1.0 atm (101325 Pa) ලෙස ගනී.
- සම්මත තත්ත්ව සංකේතවත් කරනුයේ අදාළ රාශියේ සංකේතයට දකුණු පස ඉහළින් θ ලකුණ යෙදීමෙනි.(උදා:-△Hθ , △Gθ ,△Sθ)
- සම්මත තත්ත්ව යටතේ මූලද්රව්යක ස්වභාවිකව පවතින වඩාත් ස්ථායිම ස්වරූපය එම මූලද්රව්යයේ සම්මත අවස්ථාව ලෙස හඳුන්වයි.
උදා:- N2(g) Hg(l)
Al(s) Br2(l)
පද්ධතියක සිදුවන ක්රියාවලි
ස්වයංසිද්ධ ක්රියාවලි
- ස්වයංසිද්ධ ක්රියාවලියක් යනු ස්වයංක්රීයව සිදු වන ක්රියාවලියකි.
ස්වයංසිද්ධ නොවන ක්රියාවලි
- ස්වයංසිද්ධ නොවන ක්රියාවලි යනු ස්වයංක්රීයව සිදුවීමේ ප්රවණතාවක් නෛසර්ගිකව පද්ධතිය තුළ නොමැති ක්රියාවලි ය.
ප්රතිවර්ත්ය ක්රියාවලි
- ප්රතිවර්ත්ය ක්රියාවලියක් යනු ආරම්භක අවස්ථාවක් අවසන් අවස්ථාවට පරිවර්තනය කිරීමේදී පද්ධතියක් මත සිදුකෙරෙන විපර්යාස සන්තතිය බොහෝ විට ඒ වූ ආකාරයෙන්ම ආපසු සිදු කළ හැකි විපර්යාසයකි.
අප්රතිවර්ත ක්රියාවලි
- අප්රතිවර්ත්ය ක්රියාවලියක් යනු වටපිටාවෙහි ස්ථිර වෙනසක් සිදු කිරීමෙන් තොරව පද්ධතිය යළි ආරම්භක අවස්ථාවට ගෙන ආ නොහැකි ක්රියාවලි ය.
තාප අවශෝෂක හා තාප දායක ප්රතික්රියා
- සමහර ප්රතික්රියා සිදු වන විට තාපය විමෝචනය වන අතර සමහර ප්රතික්රියා සිදුවන විට තාපය අවශෝෂණය වීමක් සිදුවේ. උදාහරණයක් ලෙස ගත් කළ ඉන්ධන දහනයේදී තාපය පිට වන අතර යූරියා ස්වල්පයක් ජලයට එකතු කළ විට එය සිසිල් වේ.
- මේ අනුව තාප විපර්යාස සිදු වන ආකාරය අනුව ප්රධාන වශයෙන් කොටස් දෙකකි.
1.තාප අවශෝෂක ප්රතික්රියා
2.තාප දායක ප්රතික්රියා
1.තාප අවශෝෂක ප්රතික්රියා :-
- ආරම්භක අවස්ථාවෙන් අවසන් අවස්ථාවට පරිවර්තනය වීමේ දී තාපය අවශෝෂණය වන ක්රියාවලි තාප අවශෝෂක ක්රියාවලි වේ. පද්ධතියේ අවසාන අවස්ථාවේදී ශක්තිය එහි ආරම්භක අවස්ථාවේදී ශක්තියට වඩා වැඩිය. අවශ්ය අමතර ශක්තිය පද්ධතිය විසින් තාපය ලෙස වටපිටාවෙන් අවශෝෂණය කරගනු ලැබේ. සාමාන්යයෙන් තාප අවශෝෂක භෞතික පරිවර්තනයකදී ආරම්භක අවස්ථාව අවසන් අවස්ථාව වෙත ගෙන ඒම සඳහා තාපය සැපයිය යුතු වේ.
2.තාප දායක ප්රතික්රියා :-
- ආරම්භක අවස්ථාවෙන් අවසාන අවස්ථාවට පරිවර්තනය වීමේදී තාපය විමෝචනය වන ක්රියාවලි තාපදායක ක්රියාවලි වේ. පද්ධතිය අවසන් අවස්ථාවේදී ශක්තිය එහි ආරම්භක අවස්ථාවේදී ශක්තියට වඩා අඩුය. අමතර ශක්තිය තාපය ලෙස වටපිටාවට නිදහස් වේ. භෞතික පරිවර්තනය තාපදායක නම් ආරම්භක අවස්ථාව අවසන් අවස්ථාව වෙත ගෙන ඒම සඳහා තාපය ඉවත් කළ යුතුය.

|
තාප අවශෝෂක ප්රතික්රියා |
තාපදායක ප්රතික්රියා |
|
ආරම්භක අවස්ථාවෙන් අවසන් අවස්ථාවට පරිවර්තනය වීමේදී තාපය අවශෝෂණය වන ක්රියාවලි තාප අවශෝෂක ක්රියාවලි වේ. |
ආරම්භක අවස්ථාවෙන් අවසන් අවස්ථාවට පරිවර්තනය වීමේදී තාපය විමෝචනය වන ක්රියාවලි තාපදායක ක්රියාවලි වේ. |
|
පද්ධතියේ අවසන් අවස්ථාවේ දී ශක්තිය එහි ආරම්භක අවස්ථාවේ ශක්තියට වඩා වැඩි ය. අවශ්ය අමතර ශක්තිය පද්ධතිය විසින් තාපය ලෙස වටපිටාවෙන් අවශෝෂණය කර ගනු ලැබේ.
උදා – ඇමෝනියම් ක්ලෝරයිඩ් ජලයේ දිය කිරිම. |
පද්ධතියේ අවසන් අවස්ථාවේ දී ශක්තිය එහි ආරම්භක අවස්ථාවේ ශක්තියට වඩා අඩු ය. අමතර ශක්තිය පද්ධතිය විසින් තාපය ලෙස වටපිටාවට නිදහස් වේ.
උදා – ඇමෝනියම් ක්ලෝරයිඩ් ජලයේ දිය කිරිම. |
|
සාමාන්යයෙන් තාපාවශෝෂක භෞතික පරිවර්තනයක දී ආරම්භක අවස්ථාව , අවසන් අවස්ථාව වෙත ගෙන ඒම සඳහා තාපය සැපයිය යුතුය.
උදා – තාපය සැපයීමෙන් ඝනයක් ද්රව බවට පත් කිරිම තාප අවශෝෂක ක්රියාවලියකි. |
භෞතික පරිවර්තනය තාපදායක නම් ආරම්භක අවස්ථාව , අවසන් අවස්ථාව වෙත ගෙන ඒම සඳහා තාපය ඉවත් කළ යුතුය.
උදා – හිමාංකයේ දී ද්රවයක් හිමායනය කිරිම තාපදායක ක්රියාවලියකි. |
|
ප්රතික්රියක + ශක්තිය (තාපය ) → ඵල \frac12{\mathrm N}_{2(\mathrm g)}+\frac12{\mathrm O}_{2(\mathrm g)}+90\mathrm{kJ}\rightarrow{\mathrm{NO}}_{(\mathrm g)}
|
ප්රතික්රියක → ඵල + ශක්තිය (තාපය) \frac12{\mathrm H}_{2(\mathrm g)}+\frac12{\mathrm O}_{2(\mathrm g)}+90\mathrm{kJ}\rightarrow{\mathrm H}_2{\mathrm O}_{(\mathrm g)\;}+242\mathrm{kJ}
|
 |
 |
|
පද්ධතිය විසින් වටපිටාවෙන් තාපය අවශෝෂණය කරගන්නා තාපාවශෝෂක ක්රියාවලියක ∆ H ධන වේ.
( එනම් ∆ H > 0 වේ. )
|
පද්ධතිය විසින් වටපිටාවට තාපය නිදහස් කරන තාපදායක ක්රියාවලියක ∆ H ඍණ වේ.
( එනම් ∆ H < 0 වේ. )
|
ශක්ති විද්යාවේ මුලික සංකල්ප හැඳින්වීම තවදුරටත්…
එන්තැල්පිය (H)
- සම්මත උෂ්ණත්ව පීඩන යටතේ දී, සංවෘත පද්ධතියක ඒකක මවුල ප්රමාණයක් ප්රතික්රියා වීමේදී පද්ධතිය විසින් පිටකරන හෝ ලබා ගන්නා තාප ප්රමාණයයි.
- මෙය විත්ති ගුණයකි.
- ද්රව්යයක එන්තැල්පිය නිරපේක්ෂව නිර්ණය කළ නොහැකි අතර, නිර්ණය කරන්නේ එන්තැල්පි වෙනසයි (∆H).
\boxed{\triangle\mathrm H\;=\;\mathrm H\;_\text{ඵල}\;-\;{\mathrm H}_\text{ප්රතික්රියක}}
නිදසුන :
C2H4(g) + 3O2(g) → 2CO(g) + 2H2O
යන ප්රතික්රියාව සඳහා 298K හා 1.00 bar පීඩනයේදී සම්මත එන්තැල්පි විපර්යාසය ගණනය කරන්න.
| CO2(g) | -393.5 kJ mol-1 |
| H2O(l) | -285.8 kJ mol-1 |
| C2H4(g) | +52.3 kJ mol-1 |

