වායු පිළිබඳ චාලක අණුක වාදය සම්බන්ධ උපකල්පන
- වායු අණු අණු අතර ආකර්ෂණ හෝ විකර්ෂණ බල ක්රියාත්මක නොවේ. එනම්, වායු අංශු එකිනෙකින් ස්වායක්තව හැසිරේ.
- වායු අණු සියලු දිශා වලට විවිධ වේග වලින් සරල රේඛීය අහඹු චලිතයක යෙදේ. වායු අණු අහඹු චලිතයේ යෙදීමේදී වායුව අන්තර්ගත භාජනයේ බිත්ති සමග ගැටීමේදී වායු පීඩනය ඇතිවේ. තවද වායු අණු අණු අතරත්, වායු අණු සහ අඩංගු භාජනයේ බිත්ති අතරත් ඇතිවන සියලුම ගැටීම් පූර්ණ වශයෙන් ප්රත්යස්ථ වේ. එනම් ගැටුම්වලදී චාලක ශක්තිය හානියක් සිදු නොවේ.
- වායු අණු අතර දුර සමඟ සැසඳීමේ දී වායු අණු වල පරිමාව නොසැලකිය හැකි තරම් කුඩා වේ. එනම්, වායු අණු ලක්ෂීය ස්කන්ධ ලෙස හැසිරෙයි.
- වායු අණු වලට විභව ශක්තියක් නැත. ඇත්තේ චාලක ශක්තියක් පමණයි.
- වායු අණු වල වල මධ්යන්ය චාලක ශක්තිය නිරපේක්ෂ උෂ්ණත්වයට අනුලෝමව සමානුපාතික වන අතර, එය වායුවේ ස්වභාවයෙන් ස්වායත්ත වේ.
- වායු අණුවල මධ්යනය චාලක ශක්තිය නිරපේක්ෂ උෂ්ණත්වය මත පමණක් රදා පවතී. දෙන ලද වායු අණුවක චාලක ශක්තිය (KE) පහත සමීකරණයෙන් ප්රකාශ වේ.
\mathrm{KE}=\frac12\mathrm{mc}^2
- වායු අංශුවකට (පරමාණු හෝ අණු) එයට අනන්ය වූ ස්කන්ධයක් හා වේගයක් ඇති බව මෙමගින් ප්රකාශ වේ.
- මෙම m යනු වායු අංශුවේ ස්කන්ධය වන අතර v යනු ප්රවේගය (හෝ වේගය) වේ.
- නියත පරිමාවෙදී වායුවක් රත් කල විට පීඩනය වැඩිවේ. එයට හේතුව වායුව රත්කල විට අංශුවල චාලක ශක්තිය වැඩි වී, ඒවා බදුනේ බිත්ති සමග සිදු කරන සංඝට්ටන වැඩි වීමෙන් වැඩි පීඩනයක් ඇති කිරීමයි.
- ඒ අනුව වායු අංශු මවුල එකක චාලක ශක්තිය හා උෂ්ණත්වය අතර සම්බන්ධතාව පහත සමිකරණයෙන් ලබා දේ.
\mathrm{KE}=\frac32\mathrm{RT}
චාලක අණුක වාදය සමීකරණය
\mathrm{PV}=\frac13\mathrm{mN}\overline{\mathrm C^2}
\begin{array}{rcl}\mathrm P\;&=&\;\;\text{පීඩනය}\;\\\mathrm V\;&=&\;\;\text{පරිමාව }\;\\\mathrm m\;&=&\;\;\text{වායු අණුවක ස්කන්ධය}\;\;\\\mathrm N\;&=&\;\;\text{වායු අණු ගණන}\;\;\\\overline{\mathrm C^2}\;&=&\;\;\text{වර්ග මධ්යන්ය වේගය}\end{array}
වායුවක මධ්යන චාලක ශක්තිය
\begin{array}{rcl}\mathrm{PV}&=&\frac13\mathrm{mN}\overline{\mathrm C^2}\\&=&\frac23\times\frac12\mathrm{mN}\overline{\mathrm C^2}\\\frac12\mathrm{mN}\overline{\mathrm C^2}&=&\mathrm E\text{ වායුවේ චාලක ශක්තිය}\\\therefore\mathrm{PV}&=&\frac23\mathrm E\\\mathrm E&=&\frac32\mathrm{PV}\\&&\end{array}
නමුත්
\begin{array}{rcl}\mathrm{PV}&=&\mathrm{nRT}\\\therefore\mathrm E&=&\frac32\mathrm{nRT}\end{array}
\begin{array}{lll}\text{වායු අණු n mol වල චාලක ශක්තිය}\;\;&=&\;\frac32\mathrm{nRT}\\\;\text{වායු අණු 1 mol වල චාලක ශක්තිය}\;&=&\;\;\frac32\mathrm{RT}\end{array}
චාලක අණුක වාදය හා වේග විශ්ලේෂණය
වර්ග මධ්යන්ය මූල වේගය සහ මධ්යන්ය වේගය
නියත උෂ්ණත්වයේ දී නිත්ය පරිමාවක් ඇති බඳුනක් තුළ අඩංගු වී ඇති අණු N සංඛ්යාවක් එකිනෙකට වෙනස් C1,C2…….,CN යන වේගයන් වලින් චලනය වන විට,
\begin{array}{rcl}\text{මධ්යන්ය වේගය}\overline{\mathrm C}&=&\frac{{\mathrm C}_1+{\mathrm C}_2+{\mathrm C}_3+\dots\dots\dots{\mathrm C}_{\mathrm N}}{\mathrm N}\end{array}
\begin{array}{rcl}\text{වර්ග මධ්යන්ය වේගය}\overline{\mathrm C^2}&=&\frac{\mathrm C_1^2+\mathrm C_2^2+\mathrm C_3^2+\cdots\cdots\cdots\mathrm C_{\mathrm N}^2}{\mathrm N}\;\text{ලෙස ලිවිය හැක}\end{array}
\begin{array}{rcl}&&\text{වර්ග මධ්යන්ය මූල වේගය}\;\sqrt{\overline{\mathrm C^2}}\;\;\text{වේ.}\end{array}
වර්ග මධ්යන්ය වේගය\begin{array}{rcl}&&\overline{\mathrm C^2}\end{array} උෂ්ණත්වය මත රඳා පවතින බව පෙන්වීම සඳහා සමීකරණයක් ව්යුත්පන්න කිරීමට චාලක අණුක සමීකරණය යොදාගත හැකිය. V පරිමාවක ඇති අංශු N ගණනක් සඳහා සමීකරණය සලකා බලමු.\mathrm P=\frac{\mathrm{mN}\overline{\mathrm C^2}}{3\mathrm V} වන බව අපි දනිමු. එම නිසා\mathrm{PV}=\frac{\mathrm{mN}\overline{\mathrm C^2}}3 ලෙස ලිවිය හැක.
\mathrm N={\mathrm{nN}}_{\mathrm A} නිසා ( NA යනු ඇවගාඩ්රෝ නියතය වන අතර n යනු මවුල ප්රමාණයයි)
\mathrm{PV}=\frac{{\mathrm{mnN}}_{\mathrm A}\overline{\mathrm C^2}\;}3\;\;\;\;\;,\;\;\;\mathrm M={\mathrm{mN}}_{\mathrm A} නිසා (M යනු මවුලික ස්කන්ධය වේ) ඉහත සමීකරණය මෙසේ ප්රතිසංවිධානය කළ හැකිය.
\mathrm{PV}=\frac{\mathrm{nM}\overline{\mathrm C^2}\;}3
\begin{array}{rcl}\text{නමුත්}\;\mathrm{PV}&=&\mathrm{nRT}\;\text{නිසා}\\\mathrm{nRT}&=&\frac13\mathrm{Mn}\overline{\mathrm C^2}\\\frac{\overline{\mathrm C^2}}3&=&\frac{\mathrm{RT}}{\mathrm M}\\\sqrt{\overline{\mathrm C^2}}&=&\frac{3\mathrm{RT}}{\mathrm M}\end{array}
1.10 නිදසුන
25°C දී H2 හා N2 වායු වල වර්ග මධ්යන්ය මූල ප්රවේගය සොයන්න.
විසඳුම.
T = 25°C = 298K
M ( H2 ) = 2.0 gmol-1 = 0. 002 kgmol-1
M( N2 ) = 28.0 gmol-1 = 0.028 kgmol-1
R = 8.314 Jmol-1K-1
\begin{array}{rcl}{\mathrm H}_2\text{සදහා }\sqrt{\overline{\mathrm C^2}}&=&\sqrt{\frac{3\mathrm{RT}}{\mathrm M}}=\sqrt{\frac{3\times8.314\mathrm{Jmol}^{-1}\mathrm K^{-1}\times298\mathrm K}{0.002\mathrm{kgmol}^{-1}}}=1927.8\mathrm{ms}^{-1}\end{array}
\begin{array}{rcl}{\mathrm N}_2\text{සදහා }\sqrt{\overline{\mathrm C^2}}&=&\sqrt{\frac{3\mathrm{RT}}{\mathrm M}}=\sqrt{\frac{3\times8.314\mathrm{Jmol}^{-1}\mathrm K^{-1}\times298\mathrm K}{0.028\mathrm{kgmol}^{-1}}}=515.2\mathrm{ms}^{-1}\end{array}
මෙම සමීකරණයෙන් තහවුරු වනුයේ යම් කිසිවක් සාම්පලයක වර්ග මධ්යන්ය මූල වේගය එම වායු සාම්පලයේ නිරපේක්ෂ උෂ්ණත්වය වර්ගමූලයට අනුලෝමව සමානුපාතික වන අතර මවුලික ස්කන්ධ එහි වර්ගමූලයට ප්රතිලෝමව සමානුපාතික වන බවයි.
\begin{array}{rcl}\sqrt{\overline{\mathrm C^2}}&\propto&\;\sqrt{\mathrm T}\\\sqrt{\overline{\mathrm C^2}}&\propto&\frac{1\;\;}{\sqrt{\mathrm M}}\;\;\;\;\;\end{array}
උෂ්ණත්ව දෙකක පවතින එකම වායුවක වර්ග මධ්යන්ය මූල වේගය සංසන්දනය
\begin{array}{rcl}\frac{\sqrt{\overline{{\mathrm C}_1^2}}}{\sqrt{\overline{{\mathrm C}_2^2}}}&=&\sqrt{\frac{{\mathrm T}_1}{{\mathrm T}_2}}\end{array}
එකම උෂ්ණත්වය වන වෙනස් වායු දෙකක වායු සාම්පලවල වර්ග මධ්යන්ය මූල වේග සංසන්දනය
\begin{array}{rcl}\sqrt{\overline{\mathrm C^2}}&=&\sqrt{\frac{3\mathrm{RT}}{\mathrm M}}\\\sqrt{\overline{\mathrm C_1^2}}&=&\sqrt{\frac{\displaystyle3\mathrm{RT}}{\displaystyle\mathrm M}}\\\sqrt{\overline{\mathrm C_2^2}}&=&\sqrt{\frac{\displaystyle3\mathrm{RT}}{\displaystyle\mathrm M}}\\\frac{\sqrt{\overline{{\mathrm C}_1^2}}}{\sqrt{\overline{{\mathrm C}_2^2}}}&=&\sqrt{\frac{{\mathrm M}_1}{{\mathrm M}_2}}\end{array}
චාලක අණුක වාදය සමීකරණය මගින් පහත දැක්වෙන පරිදි සාධනය කළ හැක.
\begin{array}{rcl}\mathrm{PV}&=&\frac13\mathrm{mN}\overline{\mathrm C^2}\\&&\\&&\;\;\end{array}
මෙම සමීකරණය දෙකෙන් බෙදා දෙකෙන් ගුණ කිරීමෙන් නැවත ප්රතිසංවිධානය කළ හැක
\begin{array}{rcl}\mathrm{PV}&=&\frac{\mathrm{mN}\overline{\mathrm C^2}}3=\frac{2\mathrm N}3\left(\frac12\mathrm m\overline{\mathrm C^2}\right)=\mathrm{nRT}\\\mathrm N\left(\frac{\displaystyle1}{\displaystyle2}\mathrm m\overline{\mathrm C^2}\right)&=&\frac{\displaystyle3\mathrm{nRT}}2\;\;\;\text{සහ}\\\text{එසේම}\;\frac{\displaystyle1}{\displaystyle2}\mathrm m\overline{\mathrm C^2}&=&\frac32\left(\frac{\mathrm{nR}}{\mathrm N}\right)\mathrm T=\frac32\left(\frac{\displaystyle\mathrm R}{{\mathrm N}_{\mathrm A}}\right)\mathrm T=\frac32{\mathrm K}_{\mathrm B}\mathrm T\\&&\\&&\;\;\end{array}
KB යනු බෝල්ට්ස්මාන් නියතය වේ.
KE යනු වායු අණුවක් සඳහා වූ චාලක ශක්තිය වේ.
\begin{array}{rcl}{\mathrm K}_{\mathrm E}&=&\frac32{\mathrm K}_{\mathrm B}\mathrm T\\&&\\&&\;\;\end{array}මැක්ස්වෙල් බෝල්ට්ස්මාන් ව්යාප්තිය
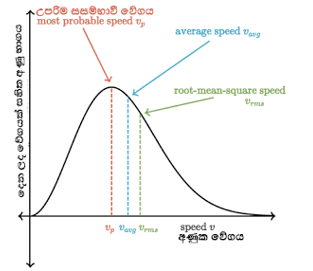
වායු සාම්පලයක වේගය විශාල පරාසයක් පුරා ව්යාප්ත වන නිසා තනි පරාමිතියකින් වේගය නිරූපණය කිරීම වෙනුවට වේග ව්යාප්ති වක්රයක් ගොඩනැගීම වඩා ඵලදායි බව මැක්ස්වෙල් බෝල්ට්ස්මාන් අදහස් කරන ලදී.වැඩි අණු සංඛ්යාවක් සතුව පවතින වේගය උපරිම සසම්භාවි වේගය ලෙස හඳුන්වයි.
එකම වායුවක වෙනස් උෂ්ණත්ව දෙකකදී වේග ව්යාප්ති වක්ර
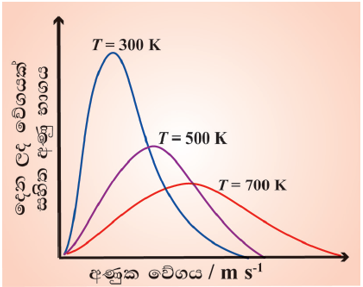
උෂ්ණත්වය වැඩිවත්ම උපරිම සසම්භාවී වේගය වැඩි වන නමුත් උපරිම සසම්භාවී වේගය අයත් කරගෙන ඇති අණු භාගය අඩු වේ.
මෙසේ වීමට හේතුව වේග ව්යාප්ති වක්රය හා X අක්ෂය අතර වර්ගඵලයෙන් සාම්පලය තුල අන්තර්ගත වන වායු අණු සංඛ්යාව නිරූපණය වන බැවින් උෂ්ණත්වය වෙනස් වුවද එය නොවෙනස්ව පැවතිය යුතු නිසාය.
එකම උෂ්ණත්වයේ පවතින මවුලික ස්කන්ධය වෙනස් වායු සාම්පල තුනක වේග ව්යාප්ති වක්ර
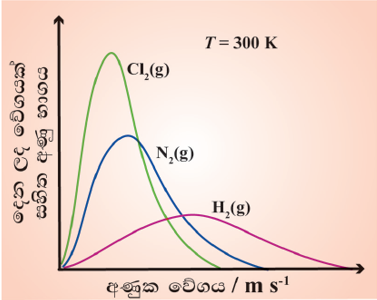
අණුක භාරය වැඩිවත්ම උපරිම සම්භාවිතා වේගය අඩු වන අතර උපරිම සම්භාවිතා වේගය අයත් කරගෙන ඇති අණු භාගය වැඩි වීම සිදුවනු ඇත.

